Vor einigen Jahren haben Forscher mit großem Erstaunen entdeckt, dass es nicht nur das berüchtigte Ozonloch in der Stratosphäre gibt, sondern dass im polaren Frühjahr Ozon auch in der Troposphäre – der untersten Schicht der Atmosphäre – völlig verschwinden kann. Warum dies so ist, war bisher nicht endgültig geklärt. Jetzt haben Wissenschaftler mithilfe von Computersimulationen den genauen Mechanismus dieses Ozonabbaus entschlüsselt. Danach kann eine Karbonatausfällung beim Gefrieren des Meerwassers eine "Bromexplosion" in Gang setzen und damit den Abbau des troposphärischen Ozons in den Polargebieten auslösen.
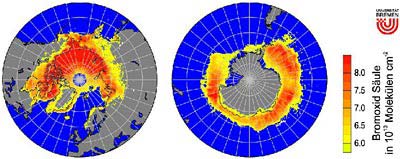
Wenn die Troposphäre ihr Ozon verliert, steigt die Konzentration von reaktivem Bromoxid über dem Meereis und in Küstennähe deutlich an. Das Ozonloch wurde deshalb von Wissenschaftlern der so genannten Bromexplosion zugeschrieben, einer Kettenreaktion ausgelöst durch Bromid-Ionen aus dem Meersalz. Klar war jedoch noch nicht, wie dieses Bromid aus dem leicht alkalischen Meerwasser in gasförmige Substanzen umgewandelt werden kann, obwohl die chemischen Reaktionen dieser Bromexplosion nur in sauren Lösungen ablaufen.
Wissenschaftler vom Max-Planck Institut für Chemie (Mainz), dem Institut für Umweltphysik (Bremen) und dem Institut für Meereskunde (Hamburg) haben nun eine neue und überzeugende Hypothese durch Computersimulationen mit dem Atmosphärenchemiemodell "MECCA" bestätigt: Wenn sich im Frühling Risse im Eis bilden, wird flüssiges Meerwasser der noch sehr kalten Luft ausgesetzt. Schnell bildet sich an der Oberfläche eine neue, dünne Eisschicht. Darüber entsteht eine flüssige Salzlake, in der die gut löslichen Salze enthalten sind. In der Kälte schlechter lösliche Salze wie Natriumsulfat und Kalziumkarbonat bleiben im Eis zurück.
Ergebnisse verbessern Verständnis des Klimasystems

Salzhaltige Teilchen – Aerosole – werden durch Aufwinde an den Rinnen im Meereis emporgehoben. Der entscheidende Punkt hierbei ist, dass die so produzierten Aerosole kaum noch Karbonat enthalten: Im Ozean puffert das Karbonat den pH-Wert im alkalischen Bereich, das karbonatarme Aerosol kann jedoch leicht angesäuert und somit die Bromexplosion in Gang gesetzt werden. Ebenfalls von Bedeutung ist, dass eine Verschiebung der chemischen Gleichgewichte bei kalten Temperaturen die Kettenreaktion begünstigt. Dies beeinflusst die Oxidationskapazität der bodennahen Luftschicht und zerstört große Mengen Ozon und führt außerdem noch zur Ablagerung von Quecksilber in den Polargebieten.
Anders als das Ozonloch in der Stratosphäre hat diese Ozonzerstörung keine direkten Auswirkungen auf unsere Gesundheit. Die neuen Erkenntnisse über die ablaufenden Reaktionen können nach Ansicht der Forscher aber zu einem besseren Verständnis des Klimasystems beitragen. Sie eröffnen auch viele neue Fragen über die zukünftige Zusammensetzung der Atmosphäre beim Abschmelzen der arktischen Meereisdecke sowie der fortschreitenden Versauerung der Ozeane.
(idw – Max-Planck-Institut für Chemie, 30.10.2006 – DLO)