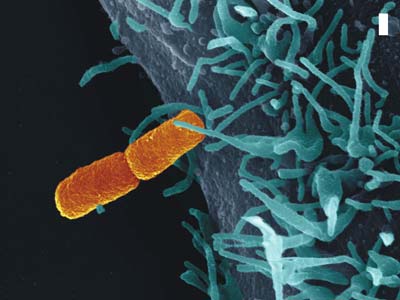
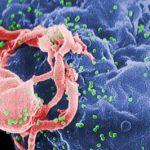
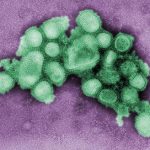
Für eine erfolgreiche Infektion müssen Mikroben das Immunsystem ihres Wirts austricksen. Dazu produzieren sie so genannte Virulenzfaktoren und leiten diese über ein Transportsystem in der Bakterienmembran nach außen. Bei einigen Erregern ist dieses Transportsystem wie eine Spritze gestaltet. Wissenschaftler haben jetzt die Mechanismen geklärt, nach denen die „Nano-Spritzen“ zusammengebaut werden.
Die neuen Erkenntnisse sind ein wichtiger Schritt für die Entwicklung von Wirkstoffen, die wesentlich früher als Antibiotika in den Verlauf einer Infektion eingreifen könnten, berichten die Forscher in der aktuellen Ausgabe der Fachzeitschrift „Nature Structural & Molecular Biology“.
Angriff der Erreger
Jeden Tag ist der menschliche Organismus dem Angriff verschiedenster Krankheitserreger ausgesetzt. Die meisten von ihnen werden dabei durch unser Immunsystem abgewehrt. Um eine erfolgreiche Infektion durchzuführen, müssen Bakterien daher die Zellen ihres Wirts manipulieren, so dass ihr eigenes Überleben gewährleistet ist. Zu diesem Zweck schleusen Mikroben über ein Transportsystem in der Bakterienmembran gezielt Virulenzfaktoren in die Wirtszelle ein.
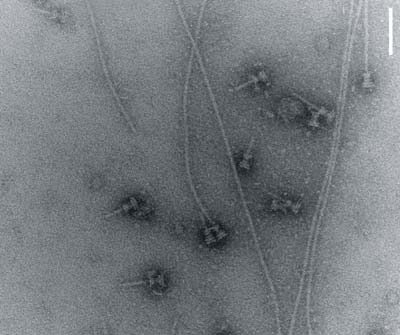
Einige Bakterien, wie die Erreger von Bakterienruhr, Lebensmittelvergiftung, Typhus und Pest, haben dabei ein besonderes Transportsystem entwickelt, das als Typ-III-Sekretionssystem bezeichnet wird. Unter dem Elektronenmikroskop sieht dieses Sekretionssystem wie eine Spritze aus, wobei der Spritzenkörper in die Bakterienmembran eingebettet ist und die Nadel nach außen weist. Die Bakterien können mit Hilfe dieser Nano-Spritzen die Virulenzfaktoren direkt in die Wirtszelle injizieren.
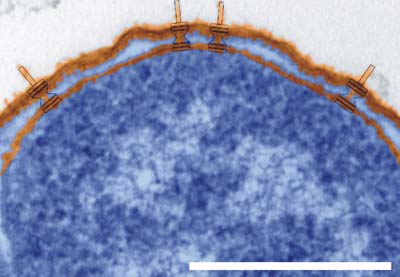
Spritzenapparat im Reagenzglas nachgebaut
Wie die Bakterien diese Nano-Spritze aufbauen, war bisher weitestgehend unbekannt. Wissenschaftler der Max-Planck-Institute für Infektionsbiologie in Berlin und für biophysikalische Chemie in Göttingen haben es jetzt zusammen mit dem Bundesamt für Materialforschung und -prüfung geschafft, grundlegende Mechanismen des Zusammenbaus der Spritze zu entschlüsseln. Diese Analysen waren möglich, weil es den Forschern gelang, den Spritzenapparat im Reagenzglas nachzubauen.
Die nähere Untersuchung dieser Vorgänge zeigte, wie die Proteine zu einer Hohlnadel zusammengebaut werden: Das Bakterium synthetisiert die Proteine in seinem Zellinneren, schleust sie durch die Spritze nach außen und setzt sie eines nach dem anderen auf die Spitze der wachsenden Nadel. Auch konnten die Wissenschaftler zeigen, dass die Proteine beim Zusammenbau der Nadel ihre räumliche Struktur ändern. Es gelang ihnen, die Strukturänderungen während des Nadelaufbaus für jede Aminosäure des Proteins genau zu verfolgen.
Antiinfektiva ohne unerwünschte Nebenwirkungen
Diese Erkenntnisse eröffnen nach Angaben der Forscher einen Ansatzpunkt für die Entwicklung von Medikamenten, die zu einem sehr frühen Zeitpunkt der Infektion wirken könnten. Diese Wirkstoffe, Antiinfektiva genannt, könnten bereits den Aufbau der Spritze und das Einschleusen von Virulenzfaktoren in die Wirtszelle verhindern.
Dies wäre ein wesentlicher Vorteil gegenüber Antibiotika, die erst durch die Membran in das Zellinnere der Bakterien müssen, um ihre Wirkung zu entfalten. Ein weiterer Nachteil von Antibiotika ist, dass diese nicht zwischen „bösen“, also krankmachenden, und guten Bakterien unterscheiden. Dies führt in der Praxis oft zu unerwünschten Nebenwirkungen. Auch das Problem der Entwicklung von Antibiotikaresistenzen könnte mit solchen Antiinfektiva umgangen werden, so die Wissenschaftler.
Strukturänderung beim Nadelprotein
Die Strukturänderung des Nadelproteins während des Spritzenaufbaus wurde durch Röntgenstrukturuntersuchungen am BESSY in Berlin und am ESRF in Grenoble sowie durch komplementäre NMR-spektroskopische Untersuchungen in flüssiger und fester Phase am Max-Planck-Institut für biophysikalische Chemie in Göttingen untersucht. Dabei verglichen die Wissenschaftler die dreidimensionale Struktur des Nadelproteins vor und nach der Entstehung der Nadel.
(idw – Max-Planck-Gesellschaft, 15.06.2010 – DLO)