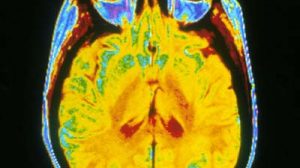
Leipziger Wissenschaftlern ist ein entscheidender Schritt für die Entwicklung eines Medikamentes gegen die Alzheimersche Krankheit gelungen. Sie konnten anhand von Versuchen mit Mäusen erstmals nachweisen, dass die Hemmung eines bestimmten Enzyms die Bildung Alzheimer-typischer Ablagerungen, so genannter Plaques, im Gehirn reduziert und dadurch die Auswirkungen der Krankheit deutlich gemildert werden. Die Forscher berichten über ihre Ergebnisse in der Fachzeitschrift „Nature Medicine“.
{1r}
Die für die Erkrankung typischen Amyloid-Plaques im Hirngewebe von Patienten wurden bereits Anfang des letzten Jahrhunderts vom Entdecker der Krankheit, Alois Alzheimer, beschrieben. „Aber erst seit reichlich zehn Jahren ist bekannt, dass sich eine bestimmte Form von kurzkettigen Eiweißen im Hirn von Alzheimer-Patienten bevorzugt ablagert“, so der Wissenschaftler Dr. Steffen Roßner vom Paul-Flechsig-Institut für Hirnforschung an der Universität Leipzig.
Bei diesen Amyloid-Eiweißen ist die randständige Aminosäure Glutamat zu einem ringförmigen pyro-Glutamat umgewandelt. „Damit sind die Eiweiße praktisch versiegelt und schwerer abbaubar“, erklärt Roßner weiter. Dies führe dazu, dass sie sich im Gehirn Betroffener anreichern, verklumpen und so genannte Fibrillen oder Oligomere bilden. Diese wiederum schädigen Nervenzellen und können im fortgeschrittenen Stadium der Erkrankung zum Verlust ganzer Neuronengruppen führen.
Verklumpung verhindert Abbau
„Darüber hinaus haben die pyro-Glutamat-modifizierten Amyloid-Eiweiße die unangenehme Eigenschaft, die eigentlich leicht abbaubaren, unveränderten Amyloid-Eiweiße gleich mit zu verklumpen und diese damit dem in der gesunden Nervenzelle fortwährend stattfindenden Abbau zu entziehen“, so Roßner. Vergleichbar sei dies mit einem stark verdichteten Schneeball, der einen verschneiten Hang hinabrollt und dabei größer und größer wird.
Während der auf dem Hang liegende Schnee bei Sonneneinstrahlung schnell abtaut, widersetzt sich die große Schneekugel sehr lange der Schmelze. Die pyro-Glutamat-modifizierten Amyloid-Eiweiße im Gehirn von Alzheimer-Patienten sind in diesem Sinne durchaus mit dem verdichteten Schneeball vergleichbar.
Plaque-Bildung im Gehirn reduziert
Bisher war allerdings unbekannt, wie es zu dieser Veränderung der Amyloid-Eiweiße kommt. In der neuen Studie konnten die Forscher nachweisen, dass das Enzym Glutaminyl-Zyklase (QC) für die krankheitsfördernde Umwandlung der Amyloid-Eiweiße verantwortlich ist.
Nach dieser Entdeckung lag nun die experimentelle Strategie auf der Hand die QC zu hemmen, um so die Plaque-Bildung im Gehirn zu reduzieren und im Idealfall zu verhindern. „Dies konnten wir im Tierversuch eindeutig nachweisen“, so Roßner.
Transgene Mäuse, die eine menschliche Erbanlage tragen, die eine vererbbare Form der Alzheimerschen Krankheit auslöst, bekamen mit dem Futter QC-Hemmer verabreicht. Dabei wurden drei Versuchsgruppen gebildet: Eine erhielt normales Futter, die zweite Gruppe eine geringe und die dritte Versuchsgruppe schließlich eine höhere Dosis des QC-Hemmers. Bei den Mäusen, die keine Hemmer bekommen hatten, ließen sich die Eiweiß-Verklumpungen in großer Zahl feststellen. Die Tiere, die den QC-Hemmer mit dem Futter aufgenommen hatten, zeigten wesentlich weniger Eiweißablagerungen, wobei bei den Mäusen, die mit der höheren Dosis behandelt worden waren, auch tatsächlich eine stärkere Wirkung zu verzeichnen war.
Weniger aktivierte Immunzellen
„Und außerdem konnten wir einen weiteren interessanten Effekt beobachten“, sagt Roßner. Die Forscher stellten nämlich fest, dass bei den behandelten Mäusen mit dem Umfang der Ablagerungen auch die Zahl der aktivierten Immunzellen im Hirn abnahm. „Dies ist eine höchst erwünschte Begleiterscheinung, denn es ist bekannt, dass die Aktivierung von Immunzellen im Hirn Entzündungsreaktionen auslöst, die wiederum zum weiteren Absterben von Nervenzellen beitragen können“, umreißt der Wissenschaftler die Bedeutung dieser Entdeckung.
Die Forscher des Paul-Flechsig-Instituts arbeiten bei ihren Untersuchungen eng mit verschiedenen weiteren Institutionen zusammen. So hatten Wissenschaftler von Probiodrug aus Halle (Saale) den Mechanismus der pyro-Glutamat Amyloid-Bildung als erste entschlüsselt und das Enzym QC als ausschlaggebend für die Bildung von Eiweiß-Ablagerungen im Gehirn von Alzheimer-Patienten identifiziert.
Viele Forscher beteiligt
Außer dem Leipziger Team testeten auch Forscher aus dem österreichischen Graz im Mäuseversuch die Wirkungen des QC-Hemmers und konnten feststellen, dass die mit den Hemmern behandelten transgenen Tiere deutlich bessere Lern- und Gedächtnisleistungen zeigten als ihre unbehandelten Artgenossen.
Andere Wissenschaftler aus Halle (Saale) untersuchten menschliches Hirngewebe beziehungsweise bestätigten die Ergebnisse in einem weiteren experimentellen Modellsystem, der Fruchtfliege Drosophila melanogaster.
Wie Roßner berichtet, beginnt nun eine weitere Phase der Erforschung der QC-Hemmer. Unter anderem sollen neue, von Probiodrug entwickelte QC-Hemmer im Tiermodell getestet werden, um Wirkstoffkandidaten für sich anschließende Klinische Studien auszuwählen.
(idw – Universität Leipzig, 30.09.2008 – DLO)