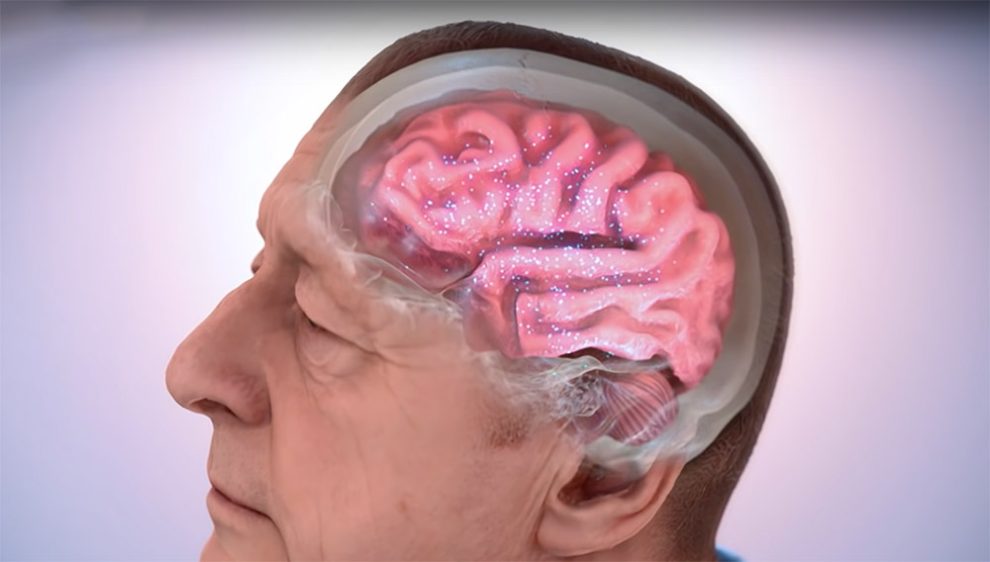
Alzheimer ist nicht gleich Alzheimer: Forschende haben fünf verschiedene Alzheimer-Subtypen identifiziert – Demenz-Varianten mit unterschiedlichen Verläufen, molekularen Ursachen und möglichen Therapieansätzen. Diese Subtypen sind an den Proteinen in der Rückenmarksflüssigkeit unterscheidbar und könnten dabei helfen, künftig gezieltere Therapien zu entwickeln, wie das Team in „Nature Aging“ berichtet. Sie liefern zudem eine Erklärung dafür, warum bisherige Alzheimer-Medikamente nur teilweise wirken.
Obwohl Alzheimer die häufigste neurologische Erkrankung im Alter ist, sind weder ihre Ursachen noch ihre neurophysiologischen Grundlagen vollständig geklärt. Das behindert auch die Entwicklung wirksamer Therapien. So bremsen die neuen Antikörper-Wirkstoffe Lecanemab und Donanemab zwar die Bildung von Amyloid-Plaques im Gehirn der Betroffenen, können das Fortschreiten der Demenz aber nur bremsen, nicht stoppen. Ein Grund dafür könnte sein, dass Alzheimer auf uneinheitliche Ursachen zurückgeht, sodass die Therapien immer nur bei einem Teil dieser Subtypen wirken.
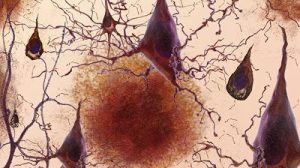
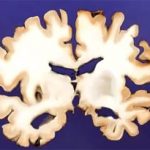
Erste Hinweise auf solche Subtypen gab es bereits: So beginnt der Abbau der Hirnzellen je nach Aktivität der Alzheimer-Risikogene in unterschiedlichen Hirnregionen. Auch bei der Anreicherung und Ausbreitung der fehlgefalteten Tau-Proteine wurden vier Subtypen entdeckt.
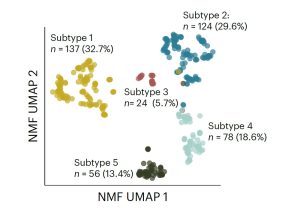
Rückenmarkspunktion enthüllt Subtypen
Jetzt gibt es neue, konkretere Daten zu den Alzheimer-Subtypen und ihren Merkmalen. Entdeckt hat sie ein Team um Betty Tijms vom Alzheimer Zentrum Amsterdam, als es die Proteine in der Rückenmarksflüssigkeit von 419 Alzheimer-Patienten und 197 gesunden Kontrollpersonen analysierte. Mithilfe der Massenspektrometrie und einer KI-gestützten Auswertung untersuchten die Forschenden, welche der insgesamt gut 3.800 Proteine im Liquor bei Alzheimer-Patienten vermehrt oder verringert vorkamen und welche Unterschiede es gab.
Es zeigte sich: 1.058 Proteine in der Rückenmarksflüssigkeit sind bei Alzheimer-Patienten signifikant verändert – und bilden dabei auffallende Gruppierungen. „Die Proteom-Profile der Alzheimer-Patienten bilden fünf Subtypen“, berichten Tijms und ihre Kollegen. Diese Subtypen unterscheiden sich in der Art und Menge der veränderten Proteine aber auch anderen Merkmalen. So ergaben ergänzende Genanalysen, dass alle fünf Subtypen neben dem bekannten Alzheimer-Risikogen APOE4-e4 ein spezifisches Muster an Risikogenvarianten besaßen.
Symptome und Fortschreiten unterschiedlich
Die fünf im Liquor identifizierten Alzheimer-Subtypen sind zudem mit spezifischen Symptomen, Fortschrittsraten der Demenz und Überlebenszeiten der Betroffenen verknüpft. „Die Subtypen unterscheiden sich beispielsweise darin, wie sie von milder kognitiver Einschränkung zur Demenz fortschreiten: Subtypen 2 und 5 haben das höchste Risiko, Subtyp 4 das geringste“, berichtet das Team. „Hirnscans mittels Magnetresonanz-Tomografie zeigten zudem, dass sich die Subtypen auch im Ausmaß und der Lage des neuronalen Abbaus unterscheiden.“
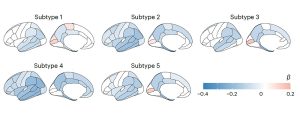
Auch im Tempo des neuronalen Abbaus gibt es Unterschiede: Patienten mit Subtyp 3 hatten die kürzeste Überlebensdauer mit im Schnitt nur rund 5,6 Jahren. Sie zeigten auch einen deutlich steileren Abfall in Gedächtnis- und Sprachtests und die höchsten Konzentrationen von fehlgefalteten Tau-Proteinen, wie Tijms und ihre Kollegen ermittelten. Betroffene mit Subtyp 1 überlebten dagegen trotz relativ hoher Tau-Protein-Werte im Liquor mit rund 8,9 Jahren nach Diagnosestellung am längsten.
Fünf verschiedene Ursachen?
Doch die neuen Daten liefern auch wertvolle Hinweise auf die molekularen und genetischen Ursachen der fünf Alzheimer-Subtypen. Wie das Team ermittelte, ist der Subtyp 1 beispielweise mit einer hohen neuronalen Plastizität verknüpft: Im Liquor dieser Patienten finden sich auffallend viele Proteine, die auf den Umbau und eine gesteigerte Aktivität von Gehirnzellen hindeuten. „Solche hyperaktiven Neuronen sekretieren mehr Tau und Amyloid und wurden vor allem im Umfeld von Plaques beobachtet“, berichten Tijms und ihre Kollegen.
Subtyp 2 ist hingegen eher durch immunspezifische Botenstoffe und Proteine gekennzeichnet. Auch einige Genvarianten dieses Subtyps sind mit Immunprozessen verknüpft. „Dies spricht dafür, dass ein überaktives angeborenes Immunsystem die Erkrankung hier verschlimmert“, so die Forschenden. Bei Alzheimer-Subtyp 3 fanden sie Hinweise auf eine Fehlregulation der RNA. Eine ähnliche Störung wurde auch schon bei der frontotemporalen Demenz beobachtet.
Beim Subtyp 4 zeigen die Patienten eine auffällige Häufung von Proteinen, die aus dem sogenannten Choroid Plexus stemmen. Dieses verzweigte Adergeflecht sitzt an den Wänden der Hirnventrikel, produziert die Hirnflüssigkeit und regelt den Transport von Stoffen durch die Blut-Hirn-Schranke. Bei Alzheimer-Patienten mit Subtyp 4 scheint diese Regulation gestört zu sein, wie Tijms und ihr Team berichten. Auch der Abbau von Hirnsubstanz ist bei diesem Typ relativ ausgeprägt. Bei Alzheimer des Subtyps 5 deuten dagegen bluttypische Protein im Liquor darauf hin, dass die Blut-Hirn-Schranke durchlässig ist und ihre Schutzfunktion nicht mehr erfüllen kann.
Neue Ansatzpunkte für Diagnose und Therapie
Nach Ansicht der Forschenden eröffnen diese Erkenntnisse wertvolle Ansätze für eine bessere Diagnose und Therapie von Alzheimer. So könnten die Unterschiede der fünf Subtypen erklären, warum bestimmte Therapien nur bei einigen Patienten anschlagen. „Angesichts der spezifischen Muster der molekularen Prozesse und genetischen Risikoprofile ist es wahrscheinlich, dass die Alzheimer-Subtypen auch spezifische Behandlungen erfordern“, schreibt das Team.
Gleichzeitig könnte die Alzheimer-Subtypen auch erklären, warum beispielsweise die Antikörper-Präparate nur bei einigen Patienten schwere Hirnödeme verursachen: Betroffene mit Subtyp 5 sind möglicherweise besonders anfällig, weil bei ihnen die Blut-Hirn-Schranke nicht richtig funktioniert. Die Kenntnis des Subtyps könnte daher auch für klinische Studien neuer Wirkstoffe und Therapien wichtig sein. (Nature Aging, 2024; doi: 10.1038/s43587-023-00550-7)
Quelle: Amsterdam University Medical Center