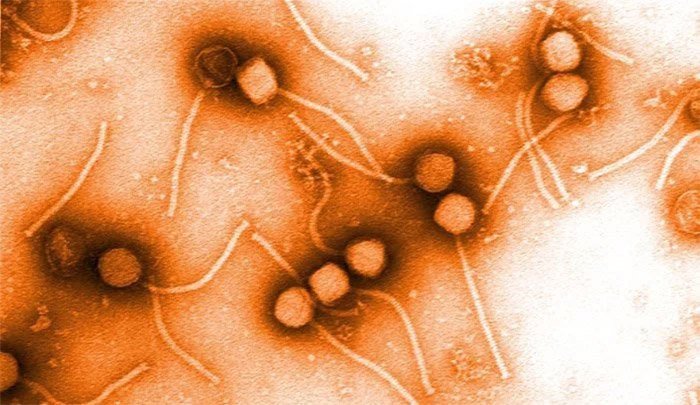
Ungewöhnliche „Bakterienfresser“: Forscher haben Phagen mit überraschend großem Erbgut entdeckt. Mit über 700.000 Basenpaaren ist das Genom eines dieser speziellen Viren das längste bekannte Phagenerbgut überhaupt. Es übersteigt sogar die Größe vieler bakterieller Genome. Spannend auch: Die großen Phagen besitzen teils Gene, die eigentlich als charakteristisch für echte Lebewesen gelten – zum Beispiel Bauanleitungen für Elemente der Proteinbiosynthese.
Auch in der Welt der Mikroorganismen treffen Forscher immer wieder auf wahre Riesen: Mikroben, die im Vergleich zu ihren Artgenossen erstaunlich groß und genetisch komplex sind. So lebt in der Nähe des Bodensees zum Beispiel ein Riesenbakterium, das gleich mehrere unterschiedliche Genome in sich trägt. Und vor Hawaii wurde jüngst ein fast bakteriengroßes Virus entdeckt.
Auf Bakterien spezialisierte Viren
Unter den Bakteriophagen gibt es ebenfalls solche überdimensionierten Vertreter. Diese Viren infizieren Bakterien, um sich zu vermehren. Aus diesem Grund gelten sie als mögliche Alternative zu Antibiotika – gleichzeitig können sie jedoch Resistenzgene auf Bakterien übertragen und dadurch Antibiotikaresistenzen erst fördern.
Der typische Phage hat eine durchschnittliche Genomgröße von rund 50.000 Basenpaaren, wie Basem Al-Shayeb von der University of California in Berkeley und seine Kollegen erklären. Doch inzwischen zeichnet sich ab: Es gibt offenbar auch Phagen, deren Erbgut aus 200.000 Basenpaaren und mehr besteht. Wie verbreitet aber sind solche großen Phagen?
735.000 Basenpaare lang
Um dies herauszufinden, haben sich die Wissenschaftler nun auf Spurensuche in fast 30 ganz unterschiedlichen Lebensräumen gemacht: Sie sammelten überall dort DNA, wo sich theoretisch Bakteriophagen tummeln könnten – von menschlichen Darmfloren über heiße Quellen, Bioreaktoren und Krankenhäuser bis hin zu Ozeanen und tiefliegenden Bodenschichten.
Die Sequenzierung der in diesen Proben gefundenen DNA zeigte, dass sich darunter tatsächlich Phagen-Erbgut befand. Insgesamt identifizierten die Forscher dabei über 300 solcher Genome mit einer Größe von über 200.000 Basenpaaren, eines war sogar 735.000 Basenpaare lang. Dieses Erbgut ist damit fast 15-mal größer als das durchschnittliche Phagen-Genom und übertrifft größentechnisch sogar viele bakterielle Genome – ein neuer Rekord, wie das Team berichtet. „Unseres Wissens nach handelt es sich um das größte bisher bekannte Phagen-Genom überhaupt.“
An der Grenze zum Leben
Das Spannende: Mit ihren großen Genomen stellen die nun gefundenen Bakteriophagen nicht nur Größenrekorde auf. Auch die darin enthalten Bauanleitungen widersprechen der Norm dessen, was Fachleute als typisch für Viren betrachten. So kodieren die Gene dieser Phagen teilweise für Elemente, die für die Proteinbiosynthese benötigt werden – darunter sogar Teile des Ribosoms, der „Proteinfabrik“ komplexer Zellen.
Doch der gängigen Annahme nach besitzen Viren weder die Gene, noch die biomolekulare Ausstattung für die Herstellung von Proteinen – stattdessen kapern sie dafür die Zellmaschinerie ihrer Wirte. „Diese großen Phagen schlagen die Brücke zwischen nicht lebenden Bakteriophagen auf der einen und Bakterien und Archaeen auf der anderen Seite“, konstatiert Al-Shayebs Kollegin Jill Banfield. Die Grenze zwischen Viren und echten Lebewesen verschwimmt damit immer mehr. Denn die Phagen sind nicht die ersten Viren, bei denen Forscher solche Gene entdeckt haben.
CRISPR im Phagengenom
Die Wissenschaftler vermuten, dass die Phagen diese Gene nutzen, um gezielt in die Tätigkeit der Ribosomen ihrer Wirte einzugreifen. Und sie haben eine weitere potenzielle genetische Waffe: Einige der großen Phagen besitzen ironischerweise auch Teile des CRISPR/Cas-Systems. Diese Genschere ist eigentlich von Bakterien bekannt, die sich damit gegen Viren wehren. Die Forscher glauben, dass die Phagen ihr CRISPR/Cas-System nutzen, um Transkriptionsfaktoren und Gene ihres Wirts auszuschalten.
Gleichzeitig könnten die CRISPR-Elemente der Phagen gemeinsam mit dem Pendant aus der bakteriellen Wirtszelle dazu dienen, viraler Konkurrenz den Garaus zu machen. Kurzum: andere Phagen zu eliminieren. „Es ist spannend zu sehen, wie diese Phagen ein System für ihre Zwecke nutzen, das für uns als typisch für Bakterien gilt“, sagt Al-Shayeb.
„Erfolgreiche Strategie“
Unter den zahlreichen Phagen-Genen sind aber auch viele, deren Funktion den Wissenschaftlern noch völlig unbekannt ist. Womöglich steckt in ihnen großes Potenzial: „Diese Gene könnten eine Quelle neuer Proteine für industrielle, medizinische oder landwirtschaftliche Zwecke sein“, konstatiert Al-Shayebs Kollege Rohan Sachdeva.
Alles in allem zeichnet sich mit der Entdeckung der neuen Bakteriophagen ab: „Phagen mit großen Genomen sind in vielen Ökosystemen der Erde vertreten. Große Genome zu haben scheint eine erfolgreiche Strategie dieser Viren zu sein – eine Strategie, über die wir noch sehr wenig wissen“, so Banfields Fazit. (Nature, 2020; doi: 10.1038/s41586-020-2007-4)
Quelle: University of California Berkeley