Hoffnung für Menschen mit Makuladegeneration: Eine Transplantation von Netzhautgewebe aus Stammzellen könnte Erblindete künftig vielleicht heilen. Forschern ist es bei Mäusen gelungen, ein solches Ersatzgewebe zu züchten und es dann erfolgreich in die zerstörte Netzhaut einzupflanzen. Erstmals ließ sich nachweisen, dass die transplantierten Zellen tatsächlich Signale an die Augennerven übermittelten.
Bei Netzhaut-Erkrankungen wie der altersbedingten Makuladegeneration (AMD) oder der Retinitis pigmentosa gehen die lichtempfindlichen Zellen der äußeren Retinaschicht zugrunde. Als Folge nimmt die Sehfähigkeit ab, bis das gesamte zentrale Sehfeld erblindet ist. In Deutschland sind von einer AMD rund zwei Millionen Menschen betroffen, sie ist die häufigste Ursache für eine Erblindung bei älteren Menschen.
Heilung durch Stammzellen?
Bisher gibt es für diese Netzhauterkrankungen keine Heilung. Das Fortschreiten lässt sich allenfalls verlangsamen, am Ende steht jedoch fast immer die Erblindung. Um dies zu ändern, suchen Wissenschaftler schon seit längerem nach Möglichkeiten, die zerstörten Netzhautzellen durch Stammzellen zu ersetzen – und so die Retina wieder zu regenerieren.
Es blieb jedoch unklar, ob solche Transplantate überhaupt anwachsen und tatsächlich das Augenlicht wiederherstellen können. „Bisher konnte noch niemand eindeutig belegen, dass transplantierte, aus Stammzellen entwickelte Retinazellen tatsächlich auf Licht reagieren“, sagt Erstautorin Michiko Mandai vom RIKEN-Forschungszentrum in Kobe. Genau dies könnte den japanischen Forschern nun gelungen sein.
Netzhautstücke gezüchtet
Für ihre Studie entnahmen die Wissenschaftler Mäusen Hautzellen und wandelten diese durch eine spezielle Behandlung in pluripotente Stammzellen zurück. Aus diesen Stammzellen züchteten sie Stücke des äußeren Netzhautgewebes – der Schicht, in der die lichtempfindlichen Sehzellen sitzen und die bei AMD zugrunde geht. Diese Gewebestücke pflanzten sie Mäusen ein, deren äußere Netzhaut bereits vollkommen zerstört war – sie waren dadurch erblindet.
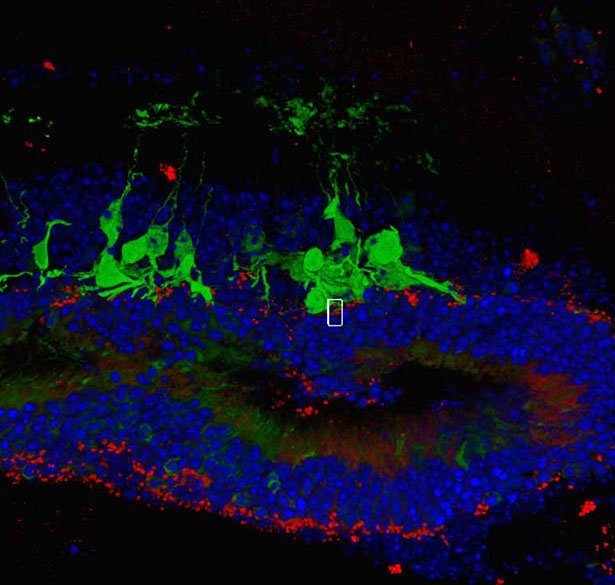
„Unsere Frage war, ob das transplantierte Gewebe auf Licht reagiert und Signale an die nachgeschalteten Neuronen in der Netzhaut der Mäuse weitergibt – im Speziellen an die retinalen Ganglienzellen, die dann die Signale ans Gehirn weitergeben“, erklären Mandai und ihre Kollegen. Um das herauszufinden, untersuchten die Forscher zum einen die Zellstruktur und Entwicklung der „geflickten“ Netzhaut. Zum anderen testeten sie, ob die Mäuse nach der Behandlung auf Licht als Warnsignal reagierten.
Angewachsen und verschaltet
Das Ergebnis: „Wir haben die Bildung von Synapsen zwischen dem transplantierten Gewebe und der restlichen Netzhaut auf direkte und bestätigte Weise nachgewiesen“, sagt Mandai. Ihre Analysen der Gewebestruktur deuten darauf hin, dass das Transplantat angewachsen und funktionsfähig ist. „Unsere Daten stützen die Annahme, dass das Lichtsignal vom eingepflanzten Gewebe zu den Zellen übermittelt wurde, die die Signale ans Gehirn senden“, so die Forscherin.
Auch die Verhaltenstests mit den behandelten Mäusen sprechen für eine erfolgreiche Transplantation, wie die Forscher berichten: Während unbehandelte Tiere keine eindeutige Reaktion auf warnende Lichtsignale zeigten, lernte die Hälfte der behandelten Mäuse schnell, einem drohenden Elektroschock auszuweichen, indem sie den beleuchteten Bereich des Käfigs mieden.
Auf den Menschen übertragbar?
Die entscheidende Frage ist jedoch, ob diese Ergebnisse bei Mäusen auf den Menschen übertragbar sind. Nach Ansicht der RIKEN-Forscher steht ihre Arbeit zwar noch am Anfang, sie sehen aber gute Chancen für eine künftige Anwendung der Transplantation auch beim Menschen. „Unsere Studie liefert den Beweis, dass das Prinzip der Transplantation von aus Stammzellen gezüchteten Netzhautgeweben funktioniert“, sagt Seniorautor Masayo Takahashi.
Ähnlich sieht es auch Marius Ader vom DFG-Forschungszentrum für regenerative Therapien in Dresden: „Die Studie stellt einen wichtigen Beitrag zur Entwicklung der Netzhautersatz-Therapie dar“, kommentiert der Retina-Spezialist. Etwas skeptischer ist Günther Zeck von der Universität Tübingen. Er räumt zwar ein, dass die Forscher ein durchaus bemerkenswertes Ergebnis erzielt haben, betont jedoch: „Es bleiben einige Fragen offen. So ist es meines Erachtens nach vollkommen offen, inwieweit die angewandte Technik auf eine Primaten-Retina übertragbar ist.“
Versuche mit menschlichen Stammzellen als nächster Schritt
Das sollen nun weitere Versuche zeigen: Als nächsten Schritt wollen die RIKEN-Forscher menschliche Stammzellen in Netzhautgewebe umwandeln und prüfen, ob dieses bei einer Transplantation in ein Tierauge ebenfalls wieder eine Lichtwahrnehmung erlaubt. „Wir wollen nach solchen zusätzlichen Tierversuchen auch erste Studien am Menschen beginnen und hoffen, dass wir auch bei Patienten mit AMD oder Retinitis pigmentosa ähnlich positive Effekte sehen.“
Ob dieser Ansatz in Zukunft tatsächlich erblindeten Menschen das Augenlicht wiedergeben kann und in welchem Maße, muss sich daher erst noch zeigen. „Eine Reaktion auf Licht ist noch nicht das Gleiche wie Sehen“, kommentiert Gerd Kempermann vom DFG-Forschungszentrum für regenerative Therapien die Studie. „Aber für Patienten wäre auch das schon mitunter ein Gewinn.“ (Stem Cell Reports, 2017; doi: 10.1016/j.stemcr.2016.12.008)
(Cell Press, 11.01.2017 – NPO)