Es dauert nur Minuten: Wenn Lithium-Ionen-Akkus überhitzen, stößt dies in ihrem Inneren eine sich hochschaukelnde thermische Reaktion an. Der Akku heizt sich dann in kürzester Zeit auf mehr als 1.000 Grad auf, wie Echtzeit-Aufnahmen des Akku-Inneren nun belegen. Je nach Konstruktion kann dann die gesamte Batterie platzen. Der Einblick in das Innenleben eines explodierenden Akkus könnte dazu beitragen, die nahezu überall eingesetzten Batterien künftig sicherer zu machen, so die Forscher im Fachmagazin „Nature Communications“.
Lithium-Ionen-Akkus stecken in Handys, Kameras und Tablets, aber auch in Elektroautos oder Flugzeugen. Hunderte Millionen der leistungsstarken Batterien werden jedes Jahr produziert und transportiert. Doch sie sind nicht ohne Risiko: Entsteht in ihrem Inneren ein Kurzschluss oder werden die Akkus von außen zu stark erhitzt, dann können sie beginnen zu brennen oder sogar explodieren.
Akkus im Hitzetest
Was bei einer überhitzten Lithium-Ionen-Akku im Inneren passiert und wie es zur Explosion kommt, haben Donal Finegan vom University College London und seine Kollegen nun erstmals in Echtzeit beobachtet und gefilmt. Im Experiment an der European Synchrotron Radiation Facility (ESRF) erhitzten sie dafür zwei verschiedene Typen von Lithium-Ionen-Akkus auf 250 Grad und beobachteten dann das Geschehen im Akku-Inneren mit Hilfe energiereicher Synchrotron Computertomografie und Wärmebildkameras.
„Wir benötigten extreme Hochgeschwindigkeits-Aufnahmen, um die thermische Kettenreaktion einzufangen – die Phase, in der die Batterie überhitzt und in Brand geraten kann“, erklärt Finegan. Einer der beiden getesteten Akkus enthielt eine zusätzliche innere Schutzhülle, die eine Explosion verhindern soll.
Hochgeschaukelt auf mehr als 1.000 Grad
Wie die Forscher berichten, dauerte es bei der ersten, intern verstärkten Batterie 168 Sekunden , bis der sogenannte thermische Runaway begann – eine sich aufschaukelnde Reaktion, durch die sich die Erhitzung im Inneren verselbstständigte. Nach kurzer Zeit war die Hitze so groß, dass das Kupfermaterial im Kern des Akkus schmolz – was auf Temperaturen von bis zu 1.000 Grad hindeute.
„Als die Nickel-Mangan-Kobalt-Elektrode exothermisch zerfiel, führte die Kombination aus lokale Gasbildung und steigenden Temperaturen zu einem rapiden Druckanstieg in der Zelle“, berichten Finegan und seine Kollegen. Nach wenigen Sekunden entlud sich dieser Druck durch ein in der Akkuwand integriertes Ventil: Ein Gasstrom, gefolgt von einer Fontäne aus geschmolzenen Bestandteilen schoss heraus.
Komplett geplatzt
Im Gegensatz dazu erreichte der zweite Akku den Moment des thermischen Runaway erst nach 217 Sekunden. Dafür aber breiteten sich Hitze und Gas in seinem Inneren so schnell aus, dass die Zelle schon eine Zehntelsekunde später explodierte. „Der Druckanstieg in Zelle 2 ließ die gesamte Kappe der Batterie abplatzen und die größtenteils nicht veränderten Akkukomponenten quollen heraus, bevor die exothermen Reaktionen zu Ende ablaufen konnten“, berichten die Forscher.
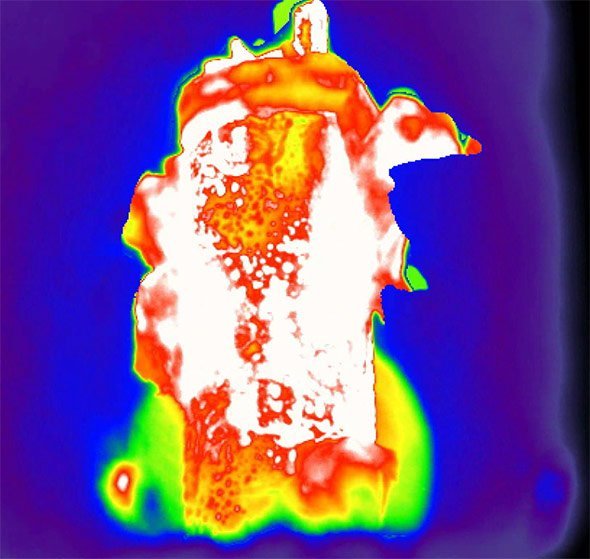
Aber was ist nun besser? Diese Frage ist offenbar auch nach dem Experiment nicht eindeutig zu beantworten. Denn wie die Forscher erklären, hält die interne Schutzhülle beim ersten Akku zwar die Reaktion im Inneren fest, erlaubt dafür aber ein extremes Hochschaukeln der Temperaturen. In einem Batteriepack könnte sich diese Hitze schnell auf andere Akkus übertragen. Zudem kann das geschmolzene Innenleben das Sicherheitsventil blockieren, so dass dann doch noch eine Explosion geschieht.
Wie geht es sicherer?
„Das frühe Austreten der Komponenten bei Zelle 2 hat den Vorteil, dass es einen weiteren Temperaturenanstieg verhindert“, sagen die Forscher. „Dadurch schützt dies die benachbarten Akkus und den Rest des Batteriepacks vor den Risiko eines thermischen Runaway.“ Dafür allerdings werden die heißen Akkubestandteile in die Gegend geschleudert und kommen so mit Sauerstoff in Kontakt, wodurch sie weiter reagieren und sich entzünden könnten.
„Die Zerstörung, die wir gesehen haben, ist unter normalen Bedingungen sehr unwahrscheinlich, denn wir haben sie Bedingungen ausgesetzt, die weit jenseits des empfohlenen Sicherheitsfensters liegen“, betont Koautor Paul Shearing vom University College London. „Aber das war entscheidend, um besser zu verstehen, wie ein Versagen solcher Akkus entsteht und sich ausbreitet.“ Die Forscher hoffen nun, dass ihre Erkenntnisse und weitere Experimente dieser Art dazu beitragen, künftige Lithium-Ionen-Akkus sicherer zu machen. (Nature Communications, 2015; doi: 10.1038/ncomms7924)
(University College London / Nature, 29.04.2015 – NPO)
















