Legendärer Pilz: Vor fast 100 Jahren entdeckte Alexander Fleming mit dem Penicillin das erste Antibiotikum. Jetzt haben Forscher erstmals das Genom seiner Schimmelpilzkultur sequenziert – der Pilze, mit denen das Zeitalter der Antibiotika begann. Die DNA-Analysen enthüllen, dass dieser Ur-Stamm zwar den heutigen Industriestämmen von Penicillium rubens sehr ähnlich ist. Dennoch gibt es einige, möglicherweise entscheidende Unterschiede.
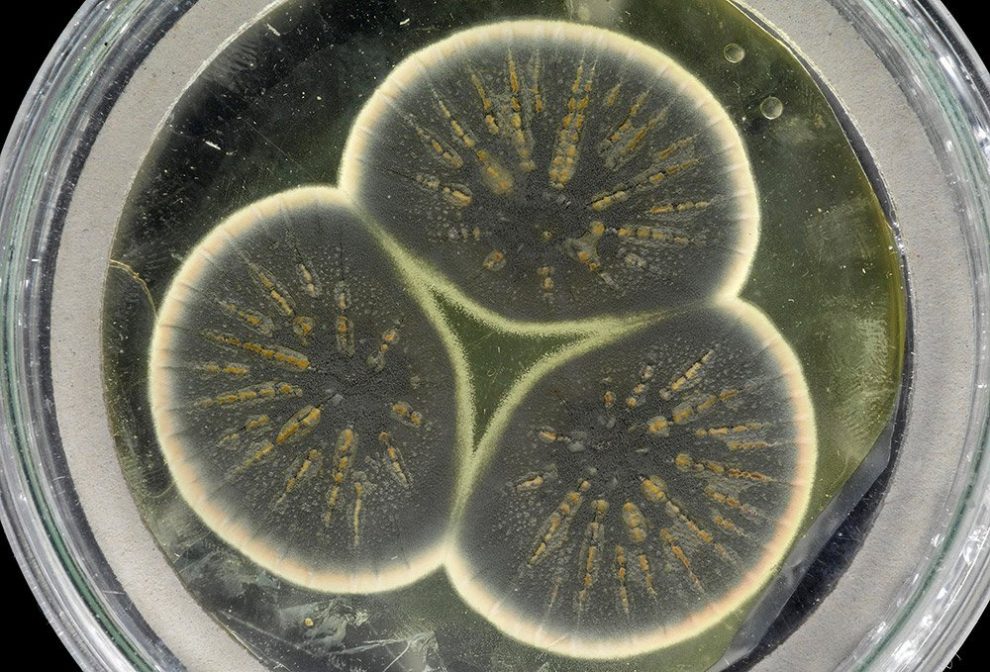
Die Ära der Antibiotika begann mit einem Zufall: 1928 ließ der britische Bakteriologe Alexander Fleming versehentlich eine Bakterienkultur mit Staphylokokken während seines Urlaubs im Labor liegen. Bei seiner Rückkehr stellt er fest, das sich ein Penicillium-Schimmelpilz auf dem Nährmedium ausgebreitet hat. Das Entscheidende jedoch: Im Umfeld des Pilzes sind alle Bakterien abgestorben. Fleming hatte den Wirkstoff Penicillin entdeckt – das erste Antibiotikum.

Reste der einst auf Flemings Petrischale gewachsenen Schimmelpilze existieren bis heute. Denn ein Teil seiner Originalkultur wurde vor gut 50 Jahren gefriergetrocknet, um diesen Stamm von Penicillium rubens für die Nachwelt zu konservieren. Für die Antibiotika-Produktion werden dagegen heute speziell gezüchtete Penicillium-Stämme eingesetzt, die eine möglichst hohe Ausbeute an Penicillin produzieren.
Erster Blick ins Erbgut von Flemings Pilzstamm
Doch nun haben britische Forscher Flemings Pilzstamm zu neuem Leben erweckt. „Eigentlich wollten wir Alexanders Flemings Penicillium für ein ganz anderes Experiment verwenden“, sagt Seniorautor Timothy Barraclough vom Imperial College London. „Doch dann stellten wir zu unserer Überraschung fest, dass noch niemand das Genom dieses Original-Penicilliums sequenziert hatte – trotz seiner historischen Bedeutung.“
Das haben Barraclough, Erstautor Ayush Pathak und ihr Team nun nachgeholt. Dafür kultivierten sie den Fleming-Stamm zunächst einige Wochen lang, bevor sie dann seine DNA isolierten und entschlüsselten. „Fast ein Jahrhundert nachdem Alexander Fleming die Wirkung des Penicillins in seinen von Penicillium rubens kontaminierten Bakterienkulturen entdeckte, berichten wir nun die erste vorläufige Genomsequenz für seinen Ursprungsstamm“, so die Forscher.
Vergleich mit Industrie-Stämmen des Penicilliums
Im nächsten Schritt untersuchten sie, ob und wie sich Flemings Stamm genetisch von zwei heute gängigen Industrie-Stämmen dieser Schimmelpilzart unterscheidet. Diese gehen auf Wildtypen von Penicillium rubens zurück, die in den 1940er-Jahren aus verschimmelten Melonen isoliert wurden. Besonderes Augenmerk richteten Pathak und sein Team bei ihrem Vergleich auf die drei Gene, über die der Pilz das Penicillin produziert.
Es zeigte sich: Zwischen Flemings Pilzkultur und den Industriestämmen von Penicillium rubens gibt es große Übereinstimmungen, aber auch einige auffallende Diskrepanzen. So sind die Gene, die den Bauplan für das Penicillin enthalten und auch diejenigen, die die Stoffwechselwege für die Penicillinproduktion regulieren, bei allen Stämmen weitgehend identisch.
Mehr Genkopien bei den US-Varianten
Unterschiede gibt es aber in der Menge und Position dieser Gene. Den Analysen zufolge besitzen die Industriestämme mehr Kopien von Teilen dieser Gene, zudem sind diese über das gesamte Erbgut verteilt. Die Wissenschaftler vermuten, dass dies die Regulation des Penicillin-Stoffwechselwegs günstig beeinflusst – und damit die höhere Ausbeute des Antibiotikums bei diesen Stämmen erklärt.
Bisher lässt sich nicht eindeutig sagen, ob diese Mutationen sich während der Zucht der Schimmelpilzkulturen angereichert haben oder aber schon bei dem US-Wildstamm vorhanden waren. Pathak und seine Kollegen vermuten aber, dass sich diese Unterschiede schon bei den Wildstämmen entwickelt haben. Sie könnten die Folge einer auf beiden Kontinenten leicht unterschiedlich wirkenden natürlichen Selektion sein.
Mögliche Helfer für bessere Antibiotika
Doch die Sequenzierung ist mehr als nur ein interessanter Ausflug in die Vergangenheit. Denn die Kenntnis des Genoms möglichst vieler Penicillium-Stämme könnte auch dazu beitragen, die altbekannten Antibiotika zu verbessern. „Die Produktion des Penicillins ist heute auf die Herstellung möglichst größer Antibiotikamengen ausgerichtet“, sagt Pathak. Aber auf dem Weg dahin könnte man einige wichtige Genmerkmale der Schimmelpilze übersehen und herausgezüchtet haben.
Der Vergleich mit alten Wildstämmen könnte daher dazu beitragen, das Penicillin möglicherweise wirksamer zu machen. „In diesem Punkt können wir von der natürlichen Selektion lernen“, so die Forscher. Denn erst das Wettrüsten von Bakterien und Schimmelpilzen habe die Bildung robuster und wirksamer Antibiotika gefördert. (Scientific Reports, 2020; doi: 10.1038/s41598-020-72584-5)
Quelle: Imperial College London