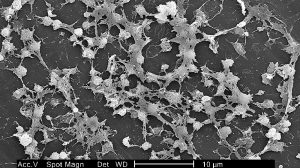
Für den Menschen können bakterielle Biofilme zu einem medizinischen Problem werden. Denn das menschliche Immunsystem hat kaum eine Chance, Krankheitserreger, die in den bakteriellen Biofilmen geschützt leben, zu bekämpfen.
Gegen Fresszellen geschützt
Wenn bakterielle Erreger in unseren Körper gelangen, bilden sie in vielen Fällen entweder selbst einen Biofilm oder heften sich an schon unserem Körper bestehenden bakteriellen Schleimschichten an. So vergrößern sich die Biofilme und bilden neue Kolonien. Das Problem: Gegen diese im Biofilm eingeschlossenen Erreger ist die menschliche Immunabwehr meist machtlos. Unsere Fresszellen können Biofilme nicht beseitigen.
Warum das so ist, haben Wissenschaftler um Carsten Matz vom Helmholtz- Zentrum für Infektionsforschung (HZI) in Braunschweig anhand von Meeresbakterien untersucht. Diese werden üblicherweise von Amöben gefressen – so wie es etwa die menschlichen Fresszellen tun.
Es zeigte sich: Solange die Bakterien frei im Wasser schwammen, waren sie leichte Beute für ihre Fressfeinde. Wurden sie jedoch sesshaft und bildeten in einem Biofilm eine Lebensgemeinschaft mit anderen Bakterien, konnten die Amöben nichts mehr gegen sie ausrichten. „Das Erstaunliche ist, dass die Einzeller, die die Biofilme attackieren, inaktiviert oder sogar getötet werden“, erklärt Matz. „Offenbar bauen Bakterien nicht nur eine Wagenburg, die schießen auch zurück.“
Und das offenbar mit harten Mitteln: Laut der Forscher setzen die Bakterien eine Art chemische Kampfstoffe gegen ihre Fressfeinde ein. Dazu produzieren die Meeresbakterien das giftige Pigment Violacein, durch das der Biofilm zart violett schimmert. Fressen die Angreifer dann nur eine einzige Zelle des Biofilms – und damit auch das Pigment in dieser Zelle – lähmt das die Amöben augenblicklich und das Violacein startet in ihnen ein Selbstmordprogramm.
Von Zahnkaries bis zur Vaginose
Das Problem: In schätzungsweise mehr als 60 Prozent aller bakteriellen Infektionskrankheiten schützen sich menschliche Krankheitserreger durch Biofilme vor unserem Immunsystem – vor allem bei chronischen Infektionen. Biofilme werden beispielsweise für die Hälfte aller Zahnerkrankungen in Verbindung gebracht.
So auch mit Karies: Die Karies verursachende Bakterienart Streptococcus mutans erzeugt auf unseren Zähnen Beläge in Form von kuppelförmigen Biofilmen, in denen sich dann hunderte andere Bakterienspezies ansiedeln und geschützt sind. Unter diesen Kuppeln können die Karies-Bakterien dann ungestört ihr Zerstörungswerk am Zahnschmelz verrichten.
Und nicht nur in unserem Mund bilden bakterielle Erreger Biofilme: Auch Wunden gewähren Bakterien die perfekten Bedingungen, ihre schützenden Schleimmatrizen herzustellen. Denn sie sind feucht und bieten den Organismen etwa durch Gewebsreste eine direkte Nahrungsquelle. Haben Bakterien einmal den Weg in eine Wunde gefunden und sich zu einer Gemeinschaft in einem Biofilm zusammengeschlossen, verhindern sie, dass sie heilt und sich wieder schließt – die Wunde wird chronisch. „Biofilme sind sehr wahrscheinlich bei allen chronischen Wunden im Spiel, auch wenn sie bisher nur in 60 bis 80 Prozent mikroskopisch nachgewiesen werden konnten“, erklärt Thomas Bjarnsholt von der Universität Kopenhagen.
Darüber hinaus spielen Biofilme auch zum Beispiel bei Harnleiterentzündungen oder bakteriellen Vaginosen, Entzündungen im Bereich der Scheide, eine Rolle. Durch Stress, hormonelle Einflüsse, ein geschwächtes Immunsystem oder übertriebene Intim-Hygiene können die dort üblicherweise lebenden Bakterien reduziert werden, sodass sich krankmachende Erreger leichter vermehren. Bei der bakteriellen Vaginose nimmt dadurch die Zahl an anaeroben Mikrobenspezies wie Gardnerella vaginalis zu, die einen Biofilm auf der Vaginalschleimhaut bilden. Die Folge können Infektionen der Gebärmutter oder des Eileiters sein. Zudem steigt das Risiko, sich mit sexuell übertragbaren Krankheiten anzustecken.
Auch Kopf und Herz gefährdet
Damit aber noch nicht genug: Bakterielle Biofilme können auch Infektionen am Nervensystem verursachen. So zum Beispiel, wenn sich nach einem Zeckenstich Borrelien im menschlichen Gewebe ausbreiten, den Körper befallen und auf das Nervensystem übergreifen. Bilden die Bakterien dort Biofilme, kann es zur chronischen Neuroborreliose kommen.
Auch das Herz ist vor bakteriellen Biofilmen nicht sicher: So kann es zum Beispiel zu einer bakteriellen Endokarditis, einer Herzinnenhautentzündung, kommen, wenn Bakterien über das Blut zum Herzen gelangen und dort an den Gefäß- und Kammerwänden ihre extrazelluläre Matrix herstellen. Zudem lassen sich Bakterien auch häufig auf den empfindlichen Herzklappen nieder und bilden dort einen Biofilm. Dort können sie dafür sorgen, dass die Herzklappen nicht mehr richtig schließen und das Herz nicht mehr effektiv pumpen kann: Es kommt zu einer Herzschwäche.
Auf Implantaten, Kathetern und Co. angesiedelt
Und nicht nur die menschlichen Organe und Gewebe sind gefährdet: Auch Fremdmaterialien, die gezielt in den menschlichen Körper eingebracht werden, stellen einen attraktiven Siedlungsplatz für Bakterien dar. So sind mehr als 45 Prozent aller Krankenhausinfektionen auf durch Biofilm verunreinigte Prothesen, Implantate und Katheter zurückzuführen, wie eine Studie von Forschern um Gregory Bixler von der Ohio State University nahegelegt hat. Die Erreger gelangen dazu entweder mit dem Einsetzen des Materials in den Körper oder aber durch eine spätere Infektion, die auch Jahre nach der Implantation einer Prothese auftreten kann.
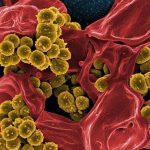
Siedeln sich auf Knochen- und Gelenkprothesen oder künstliche Herzklappen Bakterien wie meist Staphylokokken an, kommt es zu Schmerzen, Schwellungen und Überwärmung im Bereich des Implantats und die Wundheilung der Implantationsnarbe kann sich verzögern. Zudem bildet sich meist eine Fistel an der Prothese oder es kommt zu einer Blutvergiftung. Häufig muss das Ersatzgelenk oder -organ dann ausgetauscht werden.
Auch nicht dauerhaft implantiert Ersatzteile können von einer zähen Schleimmatrix befallen werden: Bilden sich etwa auf Kontaktlinsen Biofilme aus dafür typischen Bakterien wie Pseudomonas aeruginosa oder Serratia marcescens, führen sie zu Hornhautinfektionen. Diese verursachen nicht nur enorme Augenschmerzen, sondern können auch eine Sehbehinderung verursachen.