Wie der genetische Code der Lebewesen in Proteine übersetzt wird, wie also die so genannte Translation funktioniert, das glaubte man seit Jahren perfekt verstanden zu haben. Dass dies nicht stimmt, haben jetzt Frankfurter Genetiker an urtümlichen Mikroben, die in salzreichen Umgebungen leben, nachgewiesen.
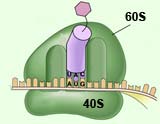
Bei diesen so genannten Archaea, die neben den zellkernlosen Bakterien und zellkerntragenden Organismen wie Tieren, Pilzen und Pflanzen die dritte Klasse von Lebewesen bilden, fanden die Forscher eine neue Art der so genannten Translationsinitiation. Dabei handelt es sich um den Mechanismus, der einem Ribosom anzeigt, an welcher Stelle der Code für eine Proteinsequenz auf der mRNA beginnt. Ribosome sind Makromoleküle, die in den Zellen die Funktion der Proteinfabriken übernehmen, die mRNA (Boten-Ribonukleinsäure oder messenger-RNA) übermittelt ihnen die in der DNA gespeicherte genetische Information zur weiteren Verarbeitung.
„Es war vollkommen unerwartet, bei einer so zentralen Funktion der Zelle wie der Translation, die seit Jahrzehnten untersucht wird, auf einen neuen Mechanismus zu stoßen“, erklärt Professor Jörg Soppa von der Universität Frankfurt, der zusammen mit seinem Team über die Ergebnisse in der angesehenen Fachzeitschrift PLoS Genetics berichtet.
Transkription und Translation
Um die in der DNA eines Lebewesens gespeicherte Information in reale Protein-Strukturen umsetzen zu können, muss die DNA zunächst in Boten-Ribonukleinsäuren (mRNAs) übersetzt werden (Transkription). In einem zweiten Schritt, der Translation, stellen dann die Ribosomen Proteine gemäß der Informationen der mRNAs her. Bisher war man davon ausgegangen, dass die Translationsinitiation bei Archaea ähnlich abläuft wie bei „normalen“ Bakterien. Dort können mRNAs mehrere für Proteine kodierende Bereiche enthalten, die jeweils durch nichtkodierende Bereiche getrennt sind. Die Information, wo die Übersetzung einer mRNA in ein Protein jeweils starten soll, ist im davor liegenden UTR (einem nicht kodierenden Bereich) lokalisiert.
Etwa drei bis zehn Nukleotide vor dem Translationsstart liegt ein nach seinen Entdeckern Shine-Dalgarno-Sequenz genanntes Motiv, das mit dem Ribosom wechselwirkt und dieses für den Beginn der Translation positioniert. Bislang wurde angenommen, dass die Shine-Dalgarno-Sequenz für die Translationsinitiation bei fast allen prokaryontischen mRNAs essentiell ist. Als Ausnahmen waren nur mRNAs bekannt, die keine 5′-UTR enthalten.
Salzliebende Archaea untersucht
Der Mechanismus der Translationsinitiation an solchen mRNAs ist bislang nur wenig untersucht worden, er unterscheidet sich allerdings deutlich von dem Mechanismus der Initiation an normalen, 5′-UTR-haltigen mRNAs. Soppas Charakterisierung von 40 mRNAs von Archaea hat nun ergeben, dass die Mehrzahl von ihnen keine 5′-UTR enthält. Untersucht wurden zwei Arten halophiler Archaea, die salzreiche Umgebungen bevorzugen.
Zumindest bei ihnen bildet der Mechanismus der Translationsregulation, der bei Bakterien als Ausnahme betrachtet wird, den Regelfall. Noch überraschender war jedoch, dass die mRNAs mit 5′-UTR keine Shine-Dalgarno Sequenz enthielten. In einer Analyse konnten die Forscher zeigen, dass dies für das gesamte Genom zutrifft und die Anwesenheit einer Shine-Dalgarno Sequenz vor einem kodierenden Bereich bei den untersuchten Arten eine Seltenheit ist. An einigen Beispielen bewiesen die Wissenschaftler außerdem, dass die 5′-UTRs ohne Shine-Dalgarno-Sequenz trotzdem in der Zelle effizient „übersetzt“ werden.
Weitere Forschungen in den nächsten Jahre sollen nun zeigen, wie dieser neue Mechanismus funktioniert, welche Komponenten beteiligt sind, und wie weit verbreitet er in anderen Archaea oder auch in Bakterien ist.
(idw – Universität Frankfurt, 09.01.2008 – DLO)