Wissenschaftler können seit einiger Zeit normale Körperzellen mithilfe eingeschleuster Gene oder Proteinfaktoren in Alleskönner-Stammzellen verwandeln. Doch die Ausbeute der Verfahren ist bislang minimal. Max-Planck-Forscher sind jetzt in Zellen von Mäusen auf eine molekulare Maschine gestoßen, die den „Reset“-Prozess effizienter macht.
Sollten sich die jüngsten Ergebnisse auf den Menschen übertragen lassen, wäre dies ein weiterer wichtiger Schritt auf dem Weg zu patienteneigenen Stammzellen, schreiben die Forscher in der Fachzeitschrift „Cell“.
Hautzellen umprogrammiert
Vor gerade einmal vier Jahren ist japanischen Forscher als Ersten geglückt, was viele Experten zuvor für unmöglich hielten: Mithilfe gentechnischer Tricks gelang es ihnen, ausgereifte Hautzellen einer Maus so umzuprogrammieren, dass sie sich wie embryonale Stammzellen verhalten und wie diese jeden der mehr als 200 Zelltypen des Körpers bilden können.
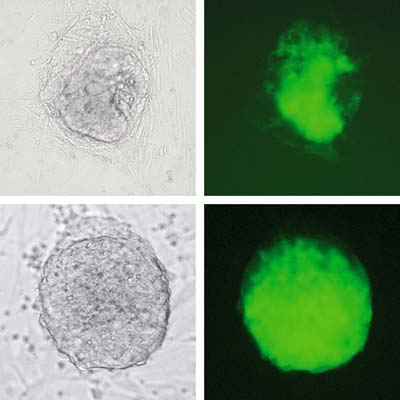
Um diese so genannten induzierten pluripotenten Stammzellen – iPS Zellen – zu erzeugen, waren weder Eizellen noch Embryonen nötig. Es genügte, vier Transgene mit „retroviral-Taxis“ in die Zellen zu bringen: Oct4, Sox2, c-Myc und Klf4. Kurz darauf zeigte sich, dass die gleiche Methode auch bei menschlichen Hautzellen funktioniert.
Seither haben sich die Verfahren deutlich verbessert. Längst kommen Forscher zum Beispiel ohne heikle „Gen-Taxis“ aus, was iPS Zellen erheblich sicherer macht. Die vier Schlüsselfaktoren, Oct4, Sox2, c-Myc und Klf4, werden heute als Proteine zugeführt.
Mühsame Prozedur
Aber die Prozedur ist nach wie vor mühsam. Nur bei einer von 10.000 Zellen gelingt im Schnitt die Verwandlung. Die wenigen gelungenen iPS Zellen müssen anschließend aus dem Zellgemisch herausgefiltert werden. Bis die Forscher pluripotente Zellen ernten können, verstreichen insgesamt drei bis vier Wochen.
Dabei weiß man seit Längerem, dass es schneller geht. Etwa, indem man eine Körperzelle mit einer pluripotenten Zelle fusioniert: Schon nach einem Tag sind dann die ersten Zellen reprogrammiert. Ähnlich effektiv ist auch der Kern-Transfer, dem das Klon-Schaf Dolly seine Existenz verdankte. Bei dem Verfahren wird der Kern einer Körperzelle in eine zuvor entkernte Eizelle verpflanzt. Rund die Hälfte der so behandelten Zellkerne ist damit nach drei bis vier Tagen reprogrammiert. Was dabei in den Zellen abläuft und den „Reset“ beschleunigt, war bislang weitgehend unklar.
Irgendetwas, vermutete der Biologe Nishant Singhal aus dem Team von Hans Schöler vom Max-Planck-Institut für molekulare Biomedizin in Münster musste also im Innern von Ei- und pluripotenten Zellen enthalten sein, das den entscheidenden Unterschied macht – und die Zellkerne wie ein Turbolader auf Neustart setzt.
Molekulare Maschinen
Singhal und seine Kollegen entwickelten deshalb ein Verfahren, mit dem sie unter allen in pluripotenten Zellen enthaltenen Proteinen jene identifizieren können, die zur Reprogrammierung beitragen und die Ausbeute an iPS Zellen erhöhen. Dabei stießen sie auf ein Set von Proteinen, das bereits als Chromatin-Remodeling-Komplex bekannt war.
Zellen von Menschen und Mäusen enthalten Hunderte unterschiedliche Varianten von diesen Protein-Komplexen. Sie alle sind molekulare Maschinen, die dazu dienen, je nach Bedarf bestimmte Abschnitte der Erbgut-DNA für so genannte Transkriptionsfaktoren zugänglich zu machen. Dabei handelt es sich um eine weitere Gruppe von Proteinen, die einzelne Gene spezifisch an- und ausschalten können.
Tatsächlich ist das gezielte Verpacken oder Öffnen bestimmter DNA-Abschnitte ein wichtiger Mechanismus, um die ganz unterschiedlichen Funktionen der Körperzellen zu steuern und dafür zu sorgen, dass in jeder Zelle das passende DNA-Programm läuft.
Deutlich höhere Ausbeute
Die Forscher um Schöler haben nun erstmals gezeigt, dass bei der Reprogrammierung der BAF Chromatin-Remodeling-Komplex eine maßgebliche Rolle spielt. Einzelne Komponenten davon, vor allem die Proteine Brg1, Baf155 und Ini1, erhöhen signifikant die Effizienz der Verwandlung von Körperzellen in Alleskönner-Stammzellen.
Mit einer Rate von bis zu 4,5 Prozent liegt die Ausbeute deutlich höher als bisher. Das war jedoch erst der Anfang: Denn nun testen die Wissenschaftler aus Münster weitere Kandidaten-Proteine, um den Prozess noch effizienter und schneller zu machen.
(idw – Max-Planck-Gesellschaft, 14.06.2010 – DLO)