Von einer winzigen Grünalge wollen sich Forscher „eine Scheibe abschneiden“: Ohne Treibhausgase kann eines ihrer Enzyme molekularen Wasserstoff produzieren – den umweltfreundlichen Kraftstoff der Zukunft. Einen Haken hat die Sache aber: Kommt Sauerstoff ins Spiel, geht die Wasserstofffabrik zugrunde, was die großtechnische Nutzung des Enzyms erschwert. Warum Sauerstoff so zerstörerisch wirkt, hat ein internationales Forscherteam jetzt auf molekularer Ebene untersucht. Ergebnis: Sauerstoffatome docken am selben Bindungsort an wie das eigentliche Substrat, der Wasserstoff.
Durch Elektronenübertragung entstehen aggressive Sauerstoffformen, die Teile des Enzymkerns attackieren. Ziel ist es nun, das Enzym gegen Sauerstoff unempfindlich zu machen. Die Wissenschaftler um Professor Thomas Happe von der Ruhr-Universität Bochum stellen zusammen mit Kollegen aus Oxford und Berlin ihre Ergebnisse in den Fachzeitschriften „Proceedings of the National Academy of Science“ (PNAS) und „Journal of the American Chemical Society“ (JACS) vor.
Wasserstoff: zukunftsträchtiger Energieträger
Molekularer Wasserstoff gilt als idealer Energieträger der Zukunft. In Kombination mit effizienten Brennstoffzellen liefert seine Verbrennung umweltfreundlich erzeugte Elektrizität. Es wird dabei keinerlei Treibhausgas frei, sondern nur reines Wasser. Wasserstoff wird allerdings bisher in großen Mengen nur aus fossilen Energieträgern wie Erdöl hergestellt.
In der Natur gibt es aber Vorbilder für eine einfache, saubere und sehr effektive Produktion von Wasserstoff. Bestimmte Proteine, so genannte Hydrogenasen, wirken als Katalysatoren und können aus Elektronen und Protonen molekularen Wasserstoff herstellen. Ein Protein kann dabei bis zu 9.000 Moleküle Wasserstoff pro Sekunde produzieren.
Grünalgen produzieren Wasserstoff bei Energieüberschuss
Diese Hydrogenasen kommen auch in Grünalgen vor, die mittels Energie aus Sonnenlicht Wasser zu Sauerstoff, Protonen (H+) und Elektronen (e-) spalten können. Dank der Hydrogenase haben die Grünalgen unter anderem die Möglichkeit, überschüssige Energie in Form von Elektronen auf Protonen zu übertragen, wobei Wasserstoff entsteht.
Happes Team erforscht die Zusammenhänge von Photosynthese und Wasserstoffproduktion am Beispiel der einzelligen Grünalge Chlamydomonas reinhardtii. Diese photosynthetisch aktiven Algen geben unter Schwefelmangelbedingungen große Mengen Wasserstoff an ihre Umgebung ab. Seit dieser Entdeckung im Jahr 2000 gilt die photobiologische Wasserstoffproduktion als viel versprechende Möglichkeit zur Herstellung von umweltfreundlichem Wasserstoff.
Der katalytisch aktive Kern
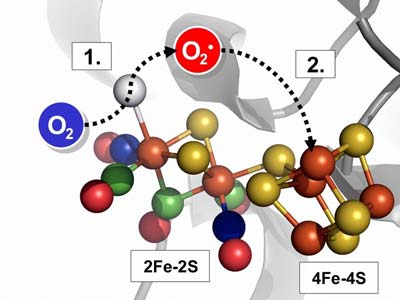
Die Forscher arbeiten an der biochemischen und biophysikalischen Charakterisierung der für die Wasserstoffproduktion verantwortlichen Enzyme. Die Hydrogenasen verfügen über einen besonderen Eisen-Schwefel-Kern – der so genannte H-Kluster -, an dem die Bildung von Wasserstoffgas mit extrem hoher Geschwindigkeit katalysiert wird. Der H-Kluster besteht aus einem Kern aus vier Eisen- und vier Schwefelatomen (4Fe-4S-Kern), der über eine Schwefelverbindung an ein weiteres Kluster mit zwei Eisen- und zwei Schwefelatomen (2Fe-2S-Kluster) gebunden ist. Dieses Subkluster besitzt ungewöhnliche Kohlenstoffmonoxid- und Cyanid-Liganden und ist der Bindungsort für den Wasserstoff.
Inaktivierung der Hydrogenase durch Sauerstoff
„Da es für die Nutzung der Hydrogenasen als biologische Katalysatoren zur Produktion von Wasserstoff gilt, ihre extreme Sauerstoffempfindlichkeit zu überwinden, fragen wir uns: Warum werden alle Hydrogenasen so schnell und irreversibel durch Luftsauerstoff inaktiviert?“, erklärt Happe. In enger Zusammenarbeit mit Kollegen aus Oxford und Berlin gelang es ihm und seinem Doktoranden Sven Stripp nun, den Mechanismus der Inaktivierung der Enzyme auf atomarer Ebene aufzuklären.
Mit Hilfe modernster biophysikalischer Methoden wie Proteinfilm-Elektrochemie und Röntgenabsorptionsspektroskopie fanden die Forscher heraus, dass das Sauerstoff-Molekül genau wie das eigentliche Substrat, der Wasserstoff, an das 2Fe-2S-Kluster gebunden wird. Allerdings geht die zerstörerische Wirkung des Sauerstoff-Moleküls offenbar nicht direkt von seiner Bindung an dieses Kluster aus. Vielmehr konnten die Forscher zeigen, dass das weiter entfernte 4Fe-4S-Cluster kurz nach der Bindung des O2-Moleküls nicht mehr nachweisbar ist, also zerstört wird.
Die Wissenschaftler postulieren, dass durch eine Übertragung von Elektronen auf den gebundenen Sauerstoff, aggressive „reaktive“ Sauerstoffvarianten – so genannte reactive oxygen species – entstehen, die dann in einer zweiten Reaktion Teile des 4Fe-4S-Kluster attackieren, dem bis dato keine Relevanz für die Sauerstoffsensitivität der Hydrogenasen zugeschrieben wurde.
Hochdurchsatz-Roboter-Technologie hilft bei der Suche
Diese Entdeckung ebnet nach Ansicht der Wissenschaftler den Weg für eine gezielte Modifikation der Hydrogenase, die sie gegenüber Luftsauerstoff unempfindlicher machen soll. „Wir arbeiten an einem viel versprechenden Ansatz, der die Prinzipien der ‚gerichteten Evolution‘ und des ‚Rationalen Protein Designs‘ kombiniert“, so Happe. Die hierbei erzeugten Enzymvarianten werden mit einem einfachen Screening-Verfahren auf erhöhte Sauerstoff-Toleranz getestet.
Auf das Arbeitsprogramm zugeschnitten wird weltweit erstmals unter Sauerstoffabschluss ein Roboter System installiert, das sowohl ein effizientes Screening der Enzymbibliotheken ermöglicht, als auch eine automatisierte Anzucht und Analyse von Kristallen sauerstoffsensibler Proteine gewährleistet, die für die Strukturaufklärung der neuen Enzyme notwendig sind.
(idw – Ruhr-Universität Bochum, 24.11.2009 – DLO)