Wenn es um die Konstruktion maßgeschneiderter Moleküle geht, arbeiten Chemiker nicht nur an einfachen geometrischen Formen wie Ringen oder Würfeln. Für viele Anwendungen sind auch miteinander verbundene oder ineinander verschachtelte Formen nötig.

Eine Frage der Energie
Kann man beispielsweise zwei molekulare Würfel ineinander verschachteln? Für eine solche Verschachtelung gibt es drei Möglichkeiten: über die Kanten, über die Ecken oder über die Flächen. Damit zwei intakte Würfel miteinander verschachtelt werden können, müssen daher Ecken oder Kanten entfernt, die Fragmente ineinandergeschoben und anschließend die Ecken oder Kanten wieder geschlossen werden. Auf molekularer Ebene geht das nur dann, wenn die Bindungen zwischen den Ecken- und Kanteneinheiten relativ schwach sind.
Aber warum sollten sich zwei oder gar mehrere Würfel freiwillig miteinander verschachteln? Wenn etwas in der Chemie freiwillig erfolgt, dann stets um den Preis, dass dabei Energie frei wird. Das ist genau dann der Fall, wenn die energetische Gesamtsituation nach der Reaktion günstiger ist als vor der Reaktion.
Gulliver und die Liliput-Fesseln
Doch um die Frage zu beantworten, muss man außerdem noch wissen, dass es neben den echten und gerichteten Bindungen innerhalb von Molekülen noch weitere, deutlich schwächere intermolekulare Wechselwirkungen gibt, beispielsweise Wasserstoffbrückenbindungen oder die noch schwächeren Dispersionswechselwirkungen. Jede Wasserstoffbrücke oder Dispersionswechselwirkung ist für sich allein genommen sehr schwach – treten sie aber gemeinsam und in Vielzahl auf, ändert sich das.
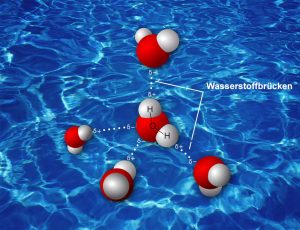
Man denke an Gullivers Reisen nach Liliput: Jeder einzelne der Fäden, mit denen die zwergenhaften Einwohner Liliputs den Riesen Gulliver fesseln, ist so klein und so schwach, dass er von Gulliver mit geringstem Kraftaufwand gelöst werden könnte – aber die Vielzahl der winzigen Fesseln sorgt dafür, dass er gefangen bleibt. Genauso ist es auch mit den vielen schwachen Wasserstoffbrückenbindungen, die Wasser bei Raumtemperatur flüssig machen. Oder mit dem Gecko, den multiple Dispersionswechselwirkungen kopfunter an der Decke haften lassen.
Auf die Bindung kommt es an
Wenn das mechanische Verschachteln zweier molekularer Würfel freiwillig gelingen soll, muss man demnach dafür Sorge tragen, dass dabei ein zusätzlicher Energiegewinn für das Molekül herausspringt. Genau das haben wir gemacht: Wir haben dafür gesorgt, dass die Eckmoleküle oder die Kantenmoleküle des Würfels Einheiten besitzen, die imstande sind, viele schwache Wechselwirkungen einzugehen.
Noch etwas konkreter: Werden beispielsweise Hydroxygruppen – typische Wasserstoffbrückenbildner – so an den Ecken des Würfels platziert, dass sie in Richtung der Würfelflächen zeigen, bilden sich zwei vierfach ineinander verschachtelte Würfel. Dafür verantwortlich sind die Wasserstoffbrücken. Werden stattdessen unpolare Methoxy- oder auch Ethylgruppen an den linearen Kanten angeboten, bilden sich dreifach verschachtelte Dimere aus zwei Würfeln oder gar Trimere aus drei Würfeln.
Diese molekulare „Bau“-Kontrolle und die Steuerung der Molekülsynthese über schwache Wechselwirkungen sind einzigartig. Sie erlauben es uns nicht nur, den hierarchischen Aufbau von biologischen Molekülen, beispielsweise die Faltung von Peptiden, besser zu verstehen – mit dieser Kenntnis können wir auch neue, noch nie da gewesene künstliche Materialien aufbauen.
Fachartikel zum Nachlesen:
Bahiru Punja Benke, Tobias Kirschbaum, Jürgen Graf, Jürgen H. Gross, Michael Mastalerz: „Dimeric and Trimeric Catenation of Giant Chiral [8+12] Imine Cubes Driven by Weak Supramolecular Interactions“, Nature Chemistry. 2023; doi: 10.1038/s41557-022-01094-w