Deutsche Wissenschaftlern haben mit bislang unerreicht hoher Auflösung den komplexen Prozess der Proteinsortierung in der Zelle untersucht. Mit Hilfe von Kryo-Elektronenmikroskopie und Einzelpartikelanalyse konnten sie dabei erstmals im Detail sichtbar machen, wie Proteinketten beim Verlassen des Ribosoms von einem Signalerkennungsprotein erkannt werden. Dieser Vorgang läuft nach den Erkenntnissen der Wissenschaftler des Berliner Max-Planck-Instituts für molekulare Genetik, der LMU München und der Universität Heidelberg bei Bakterien und höheren Organismen nach dem gleichen Mechanismus ab.
"Diese Bilder zeigen bislang unbekannte Einzelheiten auf molekularer Ebene und liefern damit die strukturelle Basis für ein detailliertes Verständnis dieser Vorgänge", so Professor Roland Beckmann vom Genzentrum der Ludwig-Maximilians- Universität (LMU) München in der aktuellen Online-Ausgabe des Wissenschaftsmagazins Nature.
Die Sortierung bestimmter Proteine in der Zelle und der Transport zu ihrem jeweiligen Bestimmungsort sind ein zentraler Schritt für die Funktion aller Organismen. Die Mehrzahl der Proteine wird bereits während ihrer Biosynthese ihrem späteren Einsatzort zugeordnet. Dies geschieht mit Hilfe eines molekularen Komplexes, der aus einem Ribosom, also der Protein-Synthese-Maschine der Zelle, und einem Signalerkennungsprotein (signal recognition particle, SRP) besteht.
Postleitzahl der Zelle
Das Schlüsselelement für die Proteinsortierung ist jedoch eine Signalsequenz, welche sich am Anfang – Wissenschaftler sprechen vom N-terminalen Ende – des vom Ribosom gebildeten Proteins befindet und quasi als "Postleitzahl" in der Zelle fungiert. Das Signalerkennungsprotein (SRP) liest diese Sequenz, sobald sie am Anfang einer gerade neu gebildeten Proteinkette das Ribosom verlässt. Im nächsten Schritt bindet SRP an das Ribosom und leitet es unter Beteiligung weiterer Komponenten an das endoplasmatischen Reticulums (ER) weiter, wo die nächsten Schritte der Sortierung erfolgen.
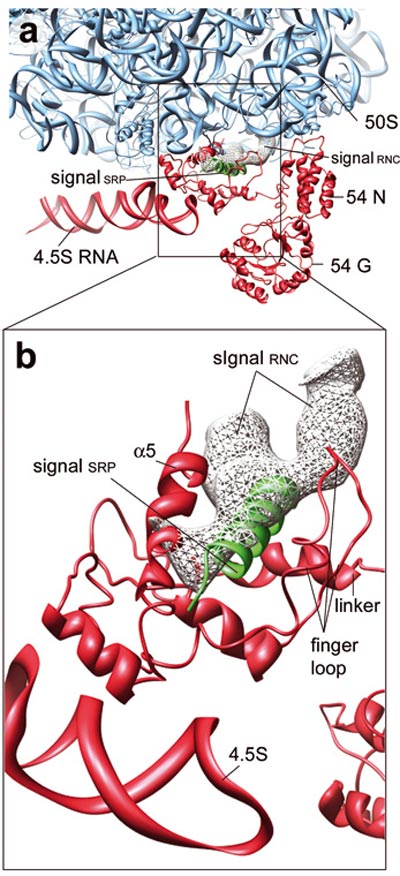
Das Wissenschaftlerteam, dem im Rahmen des Berliner UltraStrukturNetzwerk (USN) ein modernes Kryo-Elektronenmikroskop zur Verfügung steht, konnte nun in bislang unerreichter Qualität auf molekularer Ebene darstellen, wie die Signalsequenz durch SRP erkannt wird. Die Signalsequenz, die "Adresse" des Proteins, bindet an eine spezielle Bindungstasche des SRP, die so genannte M-Domäne. Diese Bindung führt zu Umlagerungen und Strukturveränderungen im SRP selber, wodurch die Überführung der Signalsequenz an den Translokon-Komplex eingeleitet werden.
Immerhin etwa 30 Prozent aller Proteine der höher entwickelten Lebewesen wie beispielsweise des Menschen werden mit diesem Mechanismus sortiert – vor allem sekretorische Proteine, beispielsweise Antikörper, und Membranproteine, die unter anderem als Empfängermoleküle für neuronale Botenstoffe oder andere Signalmoleküle dienen. Dieser Vorgang findet bei Bakterien und Säugetierzellen in vergleichbarer Weise statt. Seine Aufklärung ist ein wichtiger Baustein zum Verständnis, auf welche Weise sekretorische Proteine bzw. Membranproteinen nach ihrer Bildung in der Zelle weitergeleitet werden.
(idw – MPG/Universität München, 07.11.2006 – DLO)