Ist das Immunsystem geschwächt, können harmlose Hefepilze zur tödlichen Gefahr werden. Mit Hilfe der Next-Generation Sequenzierung können Wissenschaftler jetzt einem der häufigsten Erreger für Pilzinfektionen beim Menschen besser und schneller auf die Spur kommen. Das neue Verfahren gibt einen schnellen Einblick in das „Transkriptom“ einer Zelle – die Gesamtheit aller aktiven, abgelesenen Gene.
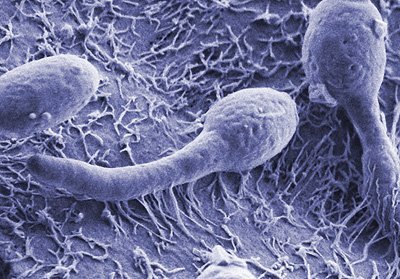
Mehr als die Hälfte aller Menschen beherbergen in ihrem Körper den Untermieter Candida albicans. Der Hefepilz ist auf der Haut, Schleimhäuten oder im Darm zu finden – oft ohne Beschwerden zu verursachen. Gefährlich wird der Pilz jedoch Patienten, deren Immunsystem geschwächt ist – etwa nach Organtransplantationen oder der Chemotherapie bei Krebs. Der Pilz dringt dann in tiefere Gewebeschichten vor und breitet sich über das Blutsystem im gesamten Körper aus. Allein in Deutschland sterben mehrere tausend Menschen im Jahr an systemischen Candida-Infektionen.
Doch warum wird Candida albicans für den Menschen lebensbedrohlich? Welche Gene sind im
pathogenen Zustand aktiv? Gibt es Wechselwirkungen zwischen Wirt und dem Pilz? Welche Schutzmechanismen des Menschen können den pathogenen Zustand verhindern? Antworten auf diese und weitere Fragen könnte das Erbgut des Pilzes liefern. Forscher des Fraunhofer-Instituts für Grenzflächen und Bioverfahrenstechnik IGB in Stuttgart haben dafür ein neues Verfahren, die so genannte Next- Generation Sequenzierungstechnologie, entwickelt.
Aktive Gene automatisiert entschlüsselt
Der große Vorteil der neuen Technik: Sie lässt sich automatisieren und beschleunigt die Analyse des
Erbguts enorm. So lässt sich innerhalb weniger Wochen zum Beispiel das Genom eines Menschen entschlüsseln und die Basenabfolge der DNA feststellen. Zum Vergleich: Fünf große Forschungszentren mit 150 Mitarbeitern arbeiteten sieben Jahre daran, um erstmals das menschliche Genom zu sequenzieren. Doch nicht nur das: Die neue Technik zeigt auch an, welche Gene zum Zeitpunkt der Analyse gerade aktiv sind und abgelesen werden. Damit können relevante Gene schneller und gezielter als bisher gefunden werden.
Über mRNA zur DNA
Forscher des IGB nutzen diese Next-Generation Sequenzierung, um herauszufinden, welche Gene am Ausbruch der Krankheit seitens des Pilzes und des Wirts beteiligt sind. Die Forscher arbeiten dazu unter anderen mit systembiologischen Ansätzen, die zur Aufklärung der wesentlichen Pathogenese-Mechanismen beitragen sollen. Zunächst isolieren die Forscher aus den humanpathogenen Hefen die mRNA – das heißt die Kopien aller aktiven Gene. Die Forscher wandeln dann die mRNA in DNA um, um diese anschließend zu fragmentieren und zu sequenzieren.
Genaktivität über Farbmarkierung sichtbar
Der Trick bei der Next-Generation Sequenzierung: Es werden nicht nur einige wenige Fragmente sequenziert, sondern Millionen DNA- Fragmente simultan. Dabei dient ein Einzelstrang der DNA als Matrize. An diesem synthetisiert ein Enzym den zweiten DNA-Strang neu – Baustein für Baustein parallel auf engstem Raum. Um diesen Prozess verfolgen zu können, ist jeder der vier verschiedenen Bausteine (die Basen: Adenin A, Guanin G, Cytosin C oder Thymin T) mit einem anderen fluorenszienden Farbstoff markiert.
Ein Detektor erfasst flächenabdeckend die unterschiedlichen Lichtsignale. So lässt sich die Basenabfolge jedes Fragments auslesen. Die enormen Datenmengen werden dann bioinformatisch ausgewertet und die Forscher können direkt erfahren, welche Gene aktiv sind.
Transkriptionsprofile von Wirt und Pilz zugleich
„Mit diesem Next-Generation-DNA-Sequenzierer lassen sich im Hochdurchsatz bis zu 100 Millionen DNA-Fragmente mit einer Leselänge von bis zu 500 Basen parallel sequenzieren“, erläutert Christian Grumaz vom IGB. „Die Methode erlaubt es erstmals, gleichzeitig hochsensitive Transkriptionsprofile von humanpathogenen Pilzen und den infizierten Wirtszellen simultan zu erhalten“, sagt Kai Sohn vom IGB. Welche riesigen Datenmengen die Next-Generation Sequenzierung liefert, zeigen sie anschaulich: In zehn Büchern ist exemplarisch das Transkriptom von Candida dokumentiert. Von der Entschlüsselung erhoffen sich Forscher entscheidende Rückschlüsse darauf, warum der Pilz gerade für bestimmte Menschen mit einem geschwächten Immunsystem so gefährlich ist.
(Fraunhofer-Gesellschaft, 23.09.2010 – NPO)