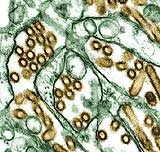
Das Vogelgrippe-Virus H5N1 existiert in zwei Varianten: Einer nicht an Säugetiere angepassten mit mildem Verlauf beim Menschen und einer veränderten, die tödliche Verläufe nach sich zieht. Jetzt haben Wissenschaftler herausgefunden, wo der entscheidende Unterschied liegt: Eine Mutation im Gen, das die virale Polymerase kodiert, ist dafür verantwortlich. Damit bieten sich neue Ansatzstellen für die Behandlung der Vogelgrippe beim Menschen, wie die Forscher in der Fachzeitschrift „American Journal of Pathology“ berichten.
H5N1 – der sich hinter diesem Kürzel verbergende Vogelgrippevirus sorgte vor einigen Jahren für Aufsehen und Besorgnis. Denn die für Vögel hochpathogene Influenza-Variante tötete nicht nur Hühner, Puten oder Gänse, er verursachte – wenn auch eher selten – höchst aggressive und tödlich verlaufende Infektionen bei Menschen. Noch hat das Virus zwar die Artschranke nicht komplett überwunden, eine Übertragung von Mensch zu Mensch ist nicht nachgewiesen, doch der Erreger verändert sich kontinuierlich. So existieren inzwischen Virenstämme, die besser an den Menschen angepasst sind und daher schwerere Krankheitsverläufe verursachen als die ursprünglich, nur an Vögel adaptierte Variante.
Jetzt haben Gülsah Gabriel vom Heinrich-Pette- Institut in Hamburg und Hans-Dieter Klenk aus dem Institut für Virologie in Marburg zwei verschiedene Virusstämme der aviären Influenza untersucht: einen an Säugetiere angepassten und einen nicht adaptierten Stamm. Sie entdeckten in Versuchen an Mäusen, dass Mutationen in einem bestimmten Gen für die erhöhte Infektiösität und Aggressivität des Virus bei Säugetieren verantwortlich ist. Die Veränderung lag in dem Gen, dass ein wichtiges Virenenzym kodiert, die virale Polymerase.
Es zeigte sich, dass der nicht-adaptierte Influenzastamm nur leichte Infektionen der Atemwege verursachte. Der Stamm mit der Genveränderung führte dagegen bei den Tieren zu einer gestörten Immunabwehr, schweren Lungenentzündungen, Infektionen des Gehirns und war tödlich. „Wir beobachten, dass bestimmte Mutationen in der viralen Polymerase die Infektiosität und die Menge von Virusnachkommen deutlich erhöhen. Hier könnte eine neuartige Therapie gegen aggressive humanpathogene Grippeviren ansetzen“, schlagen Gabriel und ihre Kollegen vor.
(Heinrich-Pette-Institut für Experimentelle Virologie und Immunologie an der Universität Hamburg (HPI), 27.08.2009 – NPO)