Forscher haben aufgeklärt, wie Bakterien das klimaschädliche Lachgas abbauen. Entscheidend dafür ist ein spezielles Enzym, das war bereits bekannt. Wie sich aber zeigte, hatte dies eine ganz andere Struktur als bisher angenommen. Die im Fachmagazin „Nature“ veröffentlichten Erkenntnisse könnte dazu beitragen, den Beitrag des Lachgases fürs Klima zukünftig genauer zu modellieren. Möglicherweise liefert es auch Ansatzstellen, um den bakteriellen Lachgasabbau zu vestärken.
Lachgas (N2O) ist ein schädliches Klimagas. Es wirkt als Treibhausgas 300-mal stärker als Kohlendioxid und zerstört die Ozonschicht. In der industriellen Landwirtschaft entsteht es auf überdüngten Feldern, wenn Mikroorganismen Nitrat-Dünger zersetzen. Der Abbau von Lachgas läuft oft unvollständig ab und hängt stark von den Umweltbedingungen ab. Forscher aus Freiburg, Konstanz und Karlsruhe KIT haben nun die Struktur und den Mechanismus des Lachgas-abbauenden Enzyms aufgeklärt.
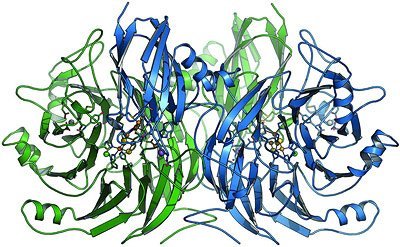
„Entscheidend war es, dass wir bei allen Untersuchungsschritten unter Ausschluss von Luftsauerstoff arbeiten konnten“, betont Walter G. Zumft vom Karlsruher Institut für Technologie. Bei Kontakt mit Sauerstoff reagieren Teile des Enzyms und es verändert seine Struktur. Die Forscher kultivierten die Bakterien daher unter einer sauerstofffreien Schutzatmosphäre. Isolierten die Enzyme in großem Maßstab, kristallisierten sie und nahmen anschließend eine Strukturanalyse mit Röntgenstrahlen vor.
Sie stellten fest, dass das Enzym N20-Reduktase aktive Zentren besitzt, welche aus vier Kupferatomen und zwei Schwefelatomen gebildet wird. „Die überraschende Erkenntnis war, dass die Mikrobiologen weltweit bislang von der falschen Struktur ausgegangen waren“, erklärt Professor Oliver Einsle, Gruppenleiter am Institut für Organische Chemie und Biochemie der Universität Freiburg. Bislang war man von nur einem Schwefelatom ausgegangen und konnte den Mechanismus des Lachgasabbaus nicht vollkommen aufklären. Die neuen Daten erlauben es, den Reaktionsablauf des Enzyms besser zu modellieren. Kommende Untersuchungen sollen weitere Details liefern und helfen zu verstehen, welchen Einfluss die Umweltbedingungen auf den Prozess haben.
„Die aktuelle Studie liefert uns einen interessanten komplementären Blick auf den Stickstoffkreislauf“, sagt Ralf Kiese vom Institut für Meteorologie und Klimaforschung des KIT. Die Lachgas- und Stickstoffproduktion auf Äckern, Weiden und in Wäldern hängt von vielen, oft gegenläufigen Effekten ab. So hat eine KIT-Studie im vergangenen Jahr gezeigt, dass unter bestimmten Bedingungen mehr Viehwirtschaft zu weniger Lachgas führen kann.
Genauere Erkenntnisse über die mikrobiellen Vorgänge und ihre Abhängigkeit von den Umweltbedingungen könnten helfen, den Beitrag des Lachgases fürs Klima besser zu modellieren. Langfristig wäre es sogar denkbar, das Wissen zu nutzen, um zu vermeiden, dass Lachgas in die Atmosphäre entweicht; etwa durch Zusatzstoffe in Düngern, die die Funktionsfähigkeit der N20-Reduktase erhalten, oder durch optimierte Prozesse in Klärwerken. (Nature, 2011; AOP; DOI:10.1038/nature10332)
(Karlsruhe Institute of Technology, 16.08.2011 – NPO)