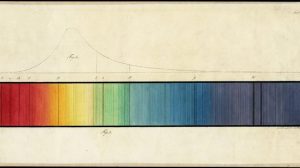
Bis das Rätsel der Fraunhofer-Linien gelöst wird, dauert es mehr als 40 Jahre: In den 1850er Jahren erforschen die Chemiker Robert Bunsen und Gustav Kirchhoff ein heute aus dem Chemieunterricht allseits bekanntes Phänomen. Sie bemerken, dass sich beim Verbrennen chemischer Elemente die Farbe der Flamme jeweils charakteristisch verändert. So färbt Natrium die Flamme beispielsweise orange. Kalium dagegen sorgt für eine violette Färbung.
Farben im Flammenlicht
Um dieses Phänomen genauer zu untersuchen, schicken die Chemiker das Flammenlicht durch ein Prisma – so wie es Fraunhofer seinerzeit mit dem Sonnenlicht getan hat. Dabei zeigt sich: Auch hier entstehen keine durchgängigen Farbbänder, sondern einzelne Lichtlinien. Diese Ergebnisse vergleichen Bunsen und Kirchhoff im Jahr 1860 mit Fraunhofers Daten und machen die entscheidende Entdeckung.
Denn sie stellen fest, dass manche Lichtlinien der Elemente genau im Bereich der schwarzen Linien des Sonnenspektrums liegen. Sie postulieren: Elemente können nicht nur spezifische Lichtlinien erzeugen, sondern diese auch schlucken. Auf der Sonne vorkommende Elemente sorgen demnach dafür, das Licht bestimmter Wellenlängen gar nicht erst die Erde erreicht. Als Folge erscheinen die schwarzen Lücken im Sonnenspektrum.
Charakteristischer Fingerabdruck
Heute kann man sich die Beobachtungen von Bunsen und Kirchhoff genauer erklären. So entsteht die Flammenfärbung, weil Elektronen durch die zugeführte Wärmeenergie kurzfristig in einen angeregten Zustand versetzt werden. Fallen sie wieder zurück, setzen sie diese Energie in Form von Licht wieder frei. Umgekehrt kann auch die Strahlungsenergie der Sonne Elektronen in einen angeregten Zustand versetzen – je nach Element sind dafür unterschiedliche Wellenlängen nötig. Das Licht dieser Wellenlängen nehmen die Elemente auf, sie absorbieren es.
Mit dem damals gängigen Atommodell können sich Kirchhoff und Bunsen diese Erklärung zwar noch nicht erschließen, dies wird erst mit dem Bohrschen Atommodell von 1913 möglich. Eines erkennen sie jedoch sehr wohl: Anhand ihres charakteristischen Fingerabdrucks im Lichtspektrum lassen sich Elemente eindeutig identifizieren.
Strahlung offenbart Geheimnisse
Das bedeutet auch: „Man konnte mit den Linien bestimmen, aus welchen chemischen Elementen ein Himmelskörper besteht, indem man seine Strahlung untersuchte“, erklärt der Wissenschaftshistoriker Jürgen Teichmann. Dieser Zusammenhang gilt nicht nur für die Sonne, in deren Spektrum mit modernen Geräten übrigens sogar 25.000 Absorptionslinien zu finden sind. Auch anderen Himmelskörpern lassen sich mithilfe von Spektrallinien Geheimnisse entlocken.
Daniela Albat
Stand: 09.11.2018