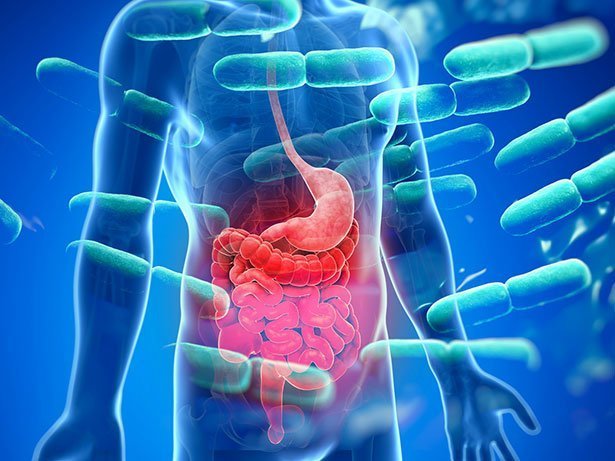
Unsere mikrobiellen Mitbewohner im Verdauungstrakt wollen vor allem eines: reichlich Futter. Sie können nur dann überleben und sich vermehren, wenn sie von uns genügend Nährstoff- Nachschub bekommen. Und dafür sorgen sie aktiver – und gezielter – als wir glauben.
{1r}
„In unserem Mikrobiom gibt es eine Vielzahl von Interessen, einige stimmen mit unseren eigenen Ernährungszielen überein, andere nicht“, erklärt Carlo Maley von der University of California in San Francisco. Um ihre Ziele zu erreichen, haben die Mikroben dabei zwei Möglichkeiten: „Sie können bei uns zum einen die Gier nach dem Essen hervorrufen, das ihnen zugutekommt. Zum anderen aber können sie unsere Stimmung so beeinflussen, dass wir zu den gewünschten Nahrungsmitteln greifen.“
Hunger und Sattheit – nur eine Frage der Mikroben?
Eine ziemlich effektive Strategie ist der Eingriff in die Kontrollsysteme, über die unser Körper Hunger und Sattheit steuert. Diese komplexen Schaltkreise sorgen dafür, dass wir nach etwas zu Essen greifen, wenn unser Blutzuckerspiegel fällt und die Energiereserven schwinden. Gleichzeitig stoppen sie unsere Esslust, bevor wir uns überfressen. Diese Kontrolle geschieht über eine Kombination aus Dehnungsrezeptoren im Magen und einer Vielzahl von Hormonen wie Leptin und Ghrelin sowie weiteren Peptidbotenstoffen.
Und genau an diesen setzen viele Darmmikroben an: Studien zeigen, dass viele von ihnen selbst Peptide produzieren können, die unseren körpereigenen Sattheits- oder Hungerboten sehr ähnlich sind. Dadurch können sie an die entsprechenden Rezeptoren andocken und uns so beispielsweise vorgaukeln, wir seien noch lange nicht satt.

Ob wir nach einem Burger satt sind oder aber Lust auf mehr haben, hängt auch von unserer Darmflora ab. © Milspa/ freeimages
Umschalten nach 20 Minuten
Wie weit der Einfluss der Darmflora in diesem Bereich reicht, demonstrierte jüngst eine Studie französischer Forscher. Sie stellten fest, dass Darmbakterien der Art Escherichia coli ihr Verhalten deutlich verändern, wenn wir eine Mahlzeit zu uns nehmen: Anfangs konsumieren sie eifrig die von uns gelieferten Nährstoffe und vermehren sich rapide. Dann jedoch, nach etwa 20 Minuten, schalten sie ihre Produktion zellulärer Abbaustoffe plötzlich um und erzeugen nun gezielt Botenstoffe, die unser Körper normalerweise nutzt, um Sattheit zu signalisieren.
Auf den ersten Blick erscheint dies kontraproduktiv: Warum sollten Bakterien freiwillig ihren Nährstoff-Nachschub unterbinden? Wie die Forscher herausfanden, kann dies für bestimmte Bakterienarten durchaus Vorteile haben. Denn haben sie sich einmal in unserem Darm etabliert, dann ist es für sie am günstigsten, wenn das Gleichgewicht der Arten möglichst stabil bleibt – und nicht etwa ein unliebsamer Konkurrent plötzlich die Oberhand gewinnt. Der Darmkeim Escherichia coli sorgt daher dafür, dass er zwar genügend Nährstoffe bekommt, verhindert aber Überschüsse, die nur den Konkurrenten zugutekommen würden.

Escherichia coli beeinflusst die Lust auf Süßes und sogar die Fähigkeit, süß zu schmecken. © greenschild/ freeimages
Lust auf Süßes
Wie groß unsere Lust auf Süßigkeiten ist, könnte ebenfalls mit dem Darmkeim Escherichia coli zusammenhängen. Denn er produziert in seiner Zellwand Zuckerverbindungen, sogenannte Lipopolysaccharide (LPS) – und diese haben offenbar einen tiefgreifenden Einfluss auf unseren Süßhunger, wie im Frühjahr 2016 ein Experiment mit Mäusen belegte.
Verabreichten Forscher ihren Mäusen eine kräftige Dosis der Bakterien-Lipopolysaccharide, reagierte deren Organismus prompt: Nach etwa fünfzehn Stunden stellten die Wissenschaftler einen erhöhten Spiegel des Sättigungshormons Leptin im Blut der Nager fest. Innerhalb einer Woche war zudem die Anzahl der Geschmacksrezeptoren auf der Zunge zurückgegangen, die auf Süßes reagieren. Als Folge hatten die Mäuse weniger Lust auf süße Nahrung.
Warum die Zellwandzucker von Escherichia coli diese Wirkung entfalten, ist unklar. Eine Erklärung wäre auch hier die Konkurrenzvermeidung: Möglicherweise benötigt der Darmkeim im Gegensatz zu anderen Darmbakterien weniger Zucker. Durch den Hemmeffekt sorgt er dafür, dass zuckerhungrigere Konkurrenten weniger Nachschub bekommen und daher weniger gut gedeihen.
Najda Podbregar
Stand: 17.06.2016