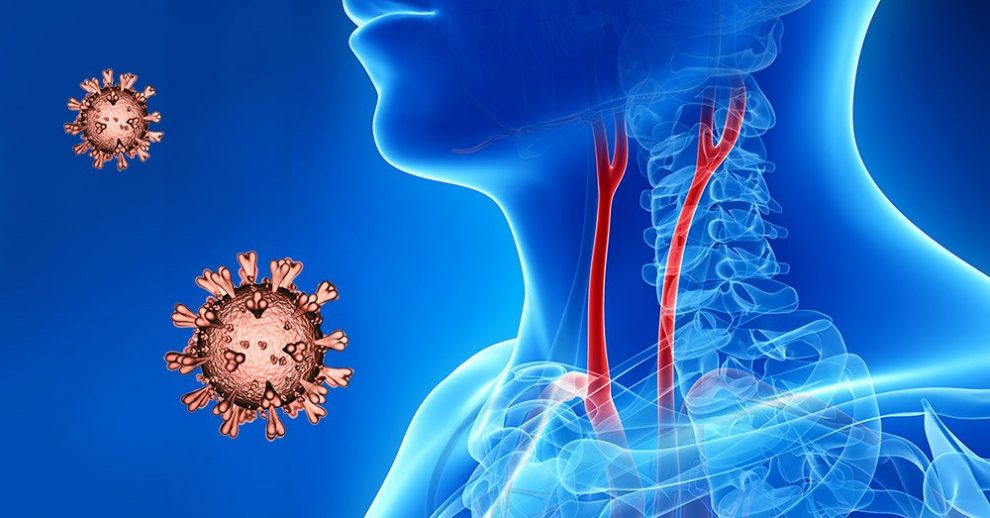
Virale Manipulation: Noch immer rätseln Mediziner über die unbemerkte Luftnot einiger Covid-19-Patienten. Jetzt gibt es eine neue Spur: Möglicherweise befällt das Coronavirus die Sensoren, die das Gasgemisch im Blut messen. Denn diese unter anderem in der Halsschlagader sitzenden Zellen tragen bei einigen Menschen viele ACE2-Rezeptoren auf ihrer Oberfläche – die Andockstellen, über die SARS-CoV-2 in unsere Zellen eindringt.
Einige Patienten mit Covid-19 leiden unter einem lebensbedrohlichen Sauerstoffmangel – bemerken es aber nicht. Obwohl sie nach Luft ringen und ohnmächtig werden müssten, bleiben die normalerweise vom Atemzentrum eingeleiteten Alarmreaktionen bei dieser „stillen Hypoxämie“ aus. Über den Grund dafür können Mediziner bislang nur spekulieren. Einige vermuten einen viralen Angriff auf das Atemzentrum, andere sehen eher eine anomale Lungenfunktion als Ursache.
Welche Rolle spielen die arteriellen O2-Sensoren?
Jetzt gibt es eine weitere Hypothese. Demnach greift das Coronavirus SARS-CoV-2 möglicherweise die Sensoren an, mit denen unser Körper den Gasgehalt des arteriellen Blutes kontrolliert. Diese unter anderem in der Halsschlagader sitzenden Chemorezeptoren geben dem Atemzentrum bei Sauerstoffmangel das Alarmsignal, das das reflexhafte Nach-Luft-Schnappen auslöst – die Reaktion, die bei der stillen Hypoxämie ausbleibt.
„Die Hemmung dieser Glomus-caroticum-Sensoren könnte eine plausible Erklärung für die ausbleibende Atemreaktion sein, die die stille Hypoxämie der Covid-19-Patienten charakterisiert“, erklären Javier Villadiego von der Universität von Sevilla und seine Kollegen. Denn die Weiterleitung der Signale aus diesen Chemorezeptoren wird von einer Reihe von regulierenden Faktoren beeinflusst – und einer davon ist das Renin-Angiotensin-System, zu dem auch das ACE2-Enzym gehört. Dieses Protein gilt als eine der Haupt-Eintrittspforten für SARS-CoV-2 beim Befall unserer Zellen.
Viele ACE2-Rezeptoren auf den Sensorzellen
Aber wie anfällig sind diese arteriellen Sauerstoffsensoren für das Virus? Um das herauszufinden, haben Villadiego und sein Team untersucht, ob und wie stark der ACE2-Rezeptor auf den Zellen des menschlichen Glomus caroticum präsent ist. Dafür führten sie ACE2-spezifische Färbungen von Gewebsschnitten mehrerer aus Autopsien stammenden Proben durch.
Das Ergebnis: „In den Glomeruli der Karotidensensoren war klar eine starke Anfärbung zu erkennen“, berichten die Forscher. „Das deutet darauf hin, dass ACE2 von den Glomuszellen produziert wird.“ In Proben von 18 gesunden, lebenden Probanden wiesen sie zudem mRNA des ACE2-Rezeptors in den Sensorzellen nach – ebenfalls ein Hinweis auf die aktive Produktion dieses Enzyms.
Angriff schon im frühen Stadium?
„Die Expression von ACE2 in den Glomeruli spricht dafür, dass diese Sauerstoff-messenden Zellen potenzielle Ziele einer Coronavirus-Infektion sein können“, schreiben Villadiego und seine Kollegen. Sie vermuten, dass das Virus schon im frühen Stadium der Infektion die Biochemie und die Mitochondrien-Funktion dieser Zellen so verändert, dass sie ihre Aufgabe nicht mehr wahrnehmen können. Tatsächlich haben Studien bereits gezeigt, dass SARS-CoV-2 die befallenen Zellen radikal umbaut.
Interessant auch: „Unsere Daten enthüllen eine große individuelle Schwankungsbreite der ACE2-Expression in diesen Geweben“, berichten die Wissenschaftler. „Das könnte erklären, warum die stille Hypoxämie scheinbar zufällig nur bei manchen Covid-19-Patienten auftritt.“
Weitere Überprüfung nötig
Noch ist all dies aber nicht viel mehr als eine Hypothese. Weitere Untersuchungen im Labor und bei Covid-19-Patienten müssen nun zeigen, ob das Coronavirus tatsächlich die arteriellen Sauerstoffsensoren angreift. „Unsere Vermutung könnte bei Autopsien von Covid-19-Patienten überprüft werden und auch durch Experimente mit transgenen Mäusen“, schlagen Villadiego und sein Team vor. (Function, 2020; doi: 10.1093/function/zqaa032)
Quelle: University of Seville