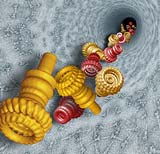
Salmonellen nutzen einen Hohlnadel-ählichen Apparat, um ihre Proteine in die Wirtzellen einzuschleusen. Jetzt haben Wissenschaftler herausgefunden, wie genau diese „Nano-Nadel“ des Bakteriums aufgebaut ist. In der aktuellen Ausgabe der Zeitschrift „Nature“ berichten sie, wie die Bakterien ihren Injektionsapparat, das so genannte "Typ III secretion system" (TTSSa), über eine raffinierte Rückkopplungsschleife regulieren.
Wie beim Aufbau dieser biologischen Nano-Maschine die genaue Länge der Nadel sichergestellt wird, konnte Dr. Thomas C. Marlovits, vom Campus Vienna Biocenter, mit Kollegen aus den USA nun klären. „Als schönes Beispiel für molekulares Multi-tasking ist das TTSSa nicht nur für den Transport von Bakterienproteinen in die Wirtszelle zuständig, sondern auch für seinen eigenen Aufbau aus gut 200 einzelnen Strukturproteinen“, erklärt Marlovits. „Dabei wird die Länge der Nadelstruktur durch einen raffinierten Mechanismus gesteuert. Kernstück dieses Mechanismus ist die Veränderung der Spezifität des TTSSa für unterschiedliche Proteine. Hat das TTSSa während der Anfangsphase des Aufbaus noch eine hohe Spezifität für seine eigenen Strukturproteine, so ändert sich diese später zu jenen Proteinen, die für den eigentlichen Infektionsprozess wichtig sind. Entscheidend für diesen Wechsel ist eine Änderung der Struktur des TTSSa."
Tatsächlich besteht das TTSSa aus vier wichtigen Bestandteilen: einer in der Bakterienmembran verankerten Basis mit einer Halterung, sowie einer darüber liegenden inneren Ringstruktur, auf der die Nadel aufgebaut wird. Marlovits konnte nun zeigen, dass die Ringstruktur die Nadel fest mit der Halterung und Basis verbindet. Diese Bindung bewirkt auch eine strukturelle Änderung der Basis, die sich auf deren Fähigkeit auswirkt, Proteine aus dem Zellinneren zu binden. Damit dient die Strukturänderung als Signal dafür, dass die Nadel fertig ist. Anstatt weiterer Proteine für den Aufbau werden dann jene Proteine transportiert, die für den Infektionsprozess notwendig sind.
Ringstruktur als Stopp-Signal
Ausschlaggebend für die Ergebnisse des Teams um Marlovits war die Kombination hochauflösender bildgebender Verfahren der Kryoelektronenmikroskopie mit der molekulargenetischen Analyse von Mutanten, die ungewöhnlich lange Nadelstrukturen bilden. Von diesen war bekannt, dass das Protein InvJ einen Einfluss auf die Nadellänge hatte aber nicht wodurch dieser Einfluss ausgeübt wurde. Marlovits Vergleich ergab ein überraschend klares Bild: den Mutanten fehlte die innere Ringstruktur komplett.
Da diese Mutanten aber trotzdem Nadelstrukturen, und zwar von enormer Länge, bilden können, lag die Vermutung nahe, dass die innere Ringstruktur eine Art Stopp-Signal für den Nadelaufbau liefert, das bei den Mutanten eben fehlt. Weitere Analysen zeigten dann zusätzlich deutliche Strukturunterschiede der Basis von Wildtyp und Mutante. Marlovits Hypothese ist nun, dass diese Strukturänderung Einfluss auf die Bindung jener Proteine hat, die durch TTSSa kanalisiert werden und so das Stopp-Signal für den Nadelaufbau liefert.
(Universität Wien, 02.06.2006 – NPO)