Blick in die Zelle: Den Nobelpreis für Medizin 2019 erhalten drei Forscher, die entdeckt haben, wie die Zellen aller tierischen Lebewesen Sauerstoff wahrnehmen – eine entscheidende Fähigkeit. Denn ohne sie würden beispielsweise unsere Muskelzellen schon bei kleinster Anstrengung absterben. Für die Identifizierung der molekularen Maschinerie hinter dieser Fähigkeit werden nun die beiden US-Amerikaner William Kaelin und Gregg Semenza sowie der Brite Sir Peter Ratcliffe ausgezeichnet.
Sauerstoff ist für alles tierische Leben essenziell. Denn dieses Molekül liefert den Zellen den Brennstoff für ihre Energiegewinnung. Es wird in den Mitochondrien gebraucht, um die energiereichen Komponenten der Nahrung in eine für die Zellen verwertbare chemische Energie in Form des Moleküls ATP umzuwandeln.
Um dies zu gewährleisten, muss der Körper diesen Prozess auch bei schwankender oder geringer Sauerstoffzufuhr aufrechterhalten können. Eine der Anpassungen daran sind beispielsweise Sauerstoffsensoren in unserer Halsschlagader. Sie sorgen dafür, dass wir automatisch schneller und tiefer atmen, wenn die Luft knapp wird. Gleichzeitig löst Sauerstoffknappheit auch die Ausschüttung des Hormons Erythropoietin (EPO) aus, das die Bildung neuer Roter Blutkörperchen fördert.
Doch wie funktioniert die Sauerstoff-Wahrnehmung auf der Ebene der Zelle? Genau dies haben die drei diesjährigen Preisträger entschlüsselt.
Vom EPO-Gen zum HIF-Komplex
Den Anfang machte Anfang der 1990er Jahre Gregg Semenza von der Johns Hopkins University in Baltimore. Als er die Genregulation für das EPO-Gen untersuchte, fand er heraus, dass diese direkt vom Sauerstoffgehalt der Zellumgebung beeinflusst wird. Zudem stellte er – gleichzeitig mit William Ratcliffe von der University of Oxford in Großbritannien – fest, dass es einen eng mit dem EPO-Gen verknüpften Sensormechanismus geben muss, der in allen Zellen und Geweben aktiv ist.
Auf der Suche nach diesem Sensor entdeckte Semenza zunächst einen Genabschnitt direkt neben dem EPO-Gen, der offenbar für die sauerstoffabhängige Reaktion verantwortlich war. Bei in Kultur gehaltenen Leberzellen fand der Forscher dann heraus, dass ein spezieller Proteinkomplex an dieses DNA-Segment bindet – und dass dieser Hypoxia Inducible Faktor Alpha (HIF-α) genannte Komplex die Genreaktion auf den Sauerstoffgehalt kontrolliert.
Damit war das erste Puzzleteil im zellulären Sauerstoffsensor gefunden. Weitere Untersuchungen enthüllten, dass HIF-α bei genügend Sauerstoff nicht lange stabil bleibt. Herrscht jedoch Sauerstoffmangel, stoppt dieser Abbau und der Gehalt dieses Proteinkomplexes in der Zelle steigt an. Das wiederum wirkt dann auf die Genregulation.
Krebsgen mit Nebenwirkungen
Das nächste Puzzleteil entdeckte 1995 William Kaelin am Dana-Farber Cancer Institute in Boston – fast durch Zufall. Denn eigentlich suchte der Krebsforscher nach der genetischen Basis einer ererbten Krebsneigung, der sogenannten Hippel-Lindau-Krankheit. Dabei stieß Kaelin auf das VHL-Gen, das in seiner mutierten Form nicht nur die Tumoranfälligkeit von Zellen beeinflusst, sondern auch die Expression von Genen, die mit der Sauerstoffverfügbarkeit verknüpft sind.
Kaelin und sein Team gingen diesem „Nebeneffekt“ nach und entdeckten eine Verbindung zum HIF-α: Das vom VHL-Gen produzierte Protein kann demnach direkt mit dem HIF-Proteinkomplex interagieren und fördert den Abbau des HIF-Moleküls bei ausreichender Sauerstoffversorgung. Die Aktivität des VHL-Gens steuert demnach, wie anfällig das HIF-α gegenüber einer Degradation ist – aber wie?
Abbaumarker in Schlüsselposition
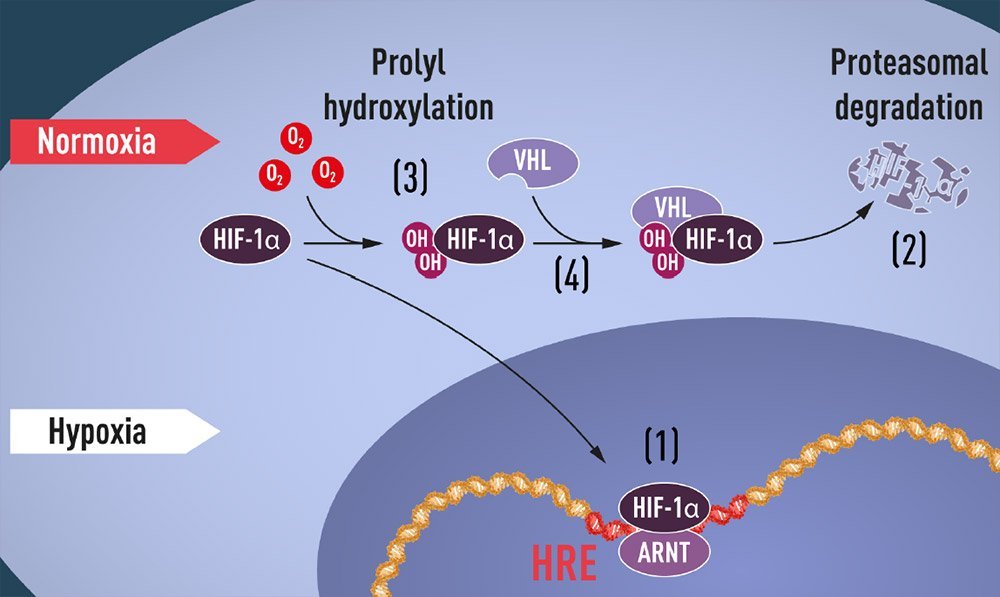
Sowohl Kaelin und sein Team als auch Ratcliffes Forschergruppe in England gingen dieser Frage nun parallel nach. 2001 dann hatten beide die Antwort gefunden: Unter normalen Bedingungen mit ausreichend Sauerstoff wird das HIF-α auf spezielle Weise markiert: Es bekommt zwei Hydroxylgruppen (-OH) an zwei Stellen seines Molekülgerüsts angehängt. Diese Anhänge wiederum ermöglichen es dem VHL-Protein anzudocken und das HIF-Molekül so für spezielle Abbauenzyme zu markieren.
Leidet die Zelle dagegen unter Sauerstoffmangel, bleibt diese Markierung aus und der Proteinkomplexx reichert sich im Zellkern an. Dort bindet er an spezielle Genabschnitte und aktiviert so die genetische Reaktion der Zelle auf die Hypoxie.
Fundamentaler Mechanismus entschlüsselt
Zusammen haben alle drei Forscher so dazu beigetragen, den komplexen Mechanismus zu entschlüsseln, über den die Zelle sich an verschiedene Sauerstoffgehalte anpassen kann. Ratcliffe, Kaelin und Semenza haben gezeigt, dass und wie sich die Genaktivität verändert, wenn Sauerstoff knapp wird oder aber reichlich vorhanden ist.
Damit haben die drei Nobelpreisträger einen fundamentalen Mechanismus erhellt, der in allen unseren Zellen vorkommt. Erst er ermöglicht es beispielsweise unseren Muskeln, sich auch bei großer Anstrengung weiter zu bewegen. Gleichzeitig erklärt er auch, wie sich Menschen an das Leben in großen Höhen anpassen konnten oder wie sich Zellen unseres Körpers auf plötzlichen Sauerstoffmangel einstellen – beispielsweise bei einem Herzinfarkt oder Schlaganfall.
Quelle: Nobelprize.org