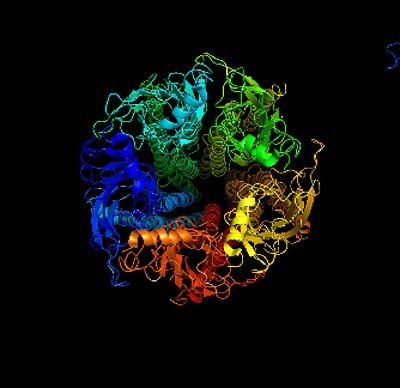
Ionenkanäle sind der Schlüssel zu jeder Nerven- und Muskelaktivität. Jetzt haben Forscher erstmals die Struktur eines solchen Kanals im geöffneten Zustand entschlüsselt. Sie stellten unter anderem fest, dass die Öffnung der fünf Untereinheiten der Bewegung einer aufgehenden Kospe gleicht. Die jetzt in „Nature“ erschienene Studie gibt damit den ersten detaillierten Einblick in einen grundlegenden Mechanismus der elektrischen Signalübertragung.
Ionenkanäle sind die elektrischen Schalter unserer Zellen. Sie ermöglichen den kontrollierten Fluss von geladenen Ionen durch die Zellmembran. Dieser Vorgang bildet die Grundlage für alle elektrisch gesteuerten Prozesse von der Nervenreizleitung bis zur Muskelbewegung. Um diese komplexen Prozesse zu ermöglichen, muss der Ionenfluss gesteuert werden. Deshalb können Ionenkanäle durch Signale kontrolliert geöffnet und geschlossen werden. Verschiedene Neurotransmitter-Rezeptoren in den Synapsen der Nervenzellen sind Teil einer Proteinfamilie von ligandenabhängigen Ionenkanälen.
In Abwesenheit des Neurotransmitters sind diese Kanäle geschlossen und versperren den Ionen den Weg durch die Membran. Werden jedoch bestimmte Neurotransmitter freigesetzt, binden diese an den Rezeptor, worauf sich der Kanal öffnet und bestimmten Ionen erlaubt, durch die Membran zu fließen. Der Proteinfamilie gehören unter anderem Acetylcholin- und GABA-Rezeptoren an, deren Fehlfunktion zu schweren Nerven- und Muskelkrankheiten führt und die wichtige Angriffspunkte für
Medikamente sind.
Geschlossener Zustand reichte nicht
„Um die Funktionsweise dieser Neurotransmitter-Rezeptoren zu verstehen, müssen wir ihre dreidimensionalen Strukturen im geschlossenen sowie im offenen Zustand kennen“, erklärt Professor Raimund Dutzler. Vor acht Monaten stellte er und seine Arbeitsgruppe am Biochemischen Institut der Universität Zürich die erste detaillierte Struktur eines geschlossenen Rezeptors vor.
Obwohl diese Struktur den Bauplan dieser Proteinfamilie zeigte, war es unmöglich, anhand einer Struktur auf den Mechanismus des Öffnens und des selektiven Ionenflusses zu schließen. Nun ist es der Gruppe gelungen, die Struktur eines verwandten Ionenkanals im offenen Zustand mithilfe der Röntgenstrukturanalyse aufzuklären. Wie bei der vorhergehenden Studie haben sich die Wissenschaftler naher bakterieller Verwandter von Neurotransmitter-Rezeptoren bedient.
„Die beiden Strukturen stammen zwar von verschiedenen Kanälen, die Proteine sind aber ähnlich genug, um die strukturelle Veränderung beim Öffnen der Pore nachvollziehen zu können“, erklärt Dutzler. Die Strukturen und Funktionsmechanismen innerhalb einer Proteinfamilie sind dabei so konserviert, dass von den Strukturen dieser bakteriellen Proteine auch auf ihre humanen Verwandten geschlossen werden kann.
Öffnung wie Knospe
„Das Ergebnis der Untersuchung ist unerwartet“, so Dutzler. „Es zeigt einen Öffnungsmechanismus, der dem traditionellen Bild dieses Prozesses widerspricht.“ Beim Öffnen bewegen sich die Teile des Proteins, die den Kanal bilden, als starre Einheit. Da das Protein aus fünf gleichen Untereinheiten besteht, die die gleichen Bewegungen ausführen, öffnet sich der Kanal ähnlich einer aufblühenden Knospe.Die Bewegungen sind dabei viel größer als erwartet, jedoch steht die Struktur im Einklang mit den Ergebnissen jahrzehntelanger experimenteller Forschung.
Laut Dutzler erlauben die beiden Strukturen Einblick in einen Mechanismus, der nun von neuen Experimenten bestätigt werden muss. Er ist überzeugt, dass die gewonnen Erkenntnisse Eingang in die Lehrbücher finden und für die Entwicklung neuer Medikamente von Neurotransmitter-Rezeptoren von grosser Bedeutung sein werden.
(Universität Zürich, 06.11.2008 – NPO)