So genannte Polyphosphatketten spielen in vielen Lebewesen eine wichtige Rolle, zum Beispiel um auch unter Mangelbedingungen Zellwachstum zu gewährleisten. Allerdings war über ihre Entstehung und Funktionsweise bisher wenig bekannt. Doch nun hat ein internationales Wissenschaftlerteam grundlegende Erkenntnisse über den Herstellungsmechanismus von Polyphosphatketten gewonnen.
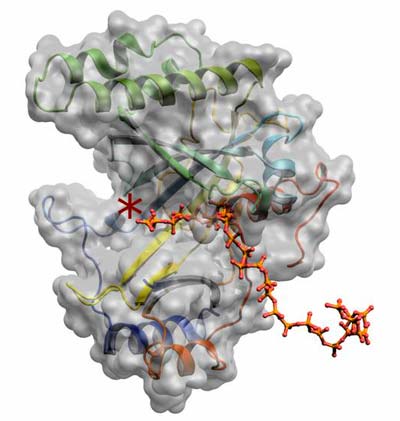
Den Forschern ist es in ihrer neuen Studie gelungen, die erste Röntgenstruktur des für den Bau verantwortlichen Enzyms aus höher entwickelten Lebewesen (Eukaryonten) zu bestimmen und wesentliche biochemische Abläufe zu charakterisieren. Aufgrund der Ergebnisse können die katalytischen Prozesse auf molekularer Ebene genau beschrieben werden.
Damit ist die Grundlage für weitere, gezielte Forschungsaktivitäten zur Rolle von Polyphosphaten geschaffen, berichten die Chemiker und Biochemiker der Ruhr-Universität Bochum (RUB) zusammen mit Forschern vom European Molecular Biology Laboratory in Heidelberg und der Universität Lausanne in „Science“.
Charakterisierung ist ein Meilenstein
Das untersuchte Enzym VTC – vacuolar transporter chaperone – verwendet die in Zellen universelle Energiewährung ATP, um daraus Schritt für Schritt Phosphatketten aufzubauen. Damit wird ein Depot angelegt, auf das der Organismus unter Stressbedingungen zurückgreifen kann. Die Forscher konnten durch Einsatz strukturbiologischer und biophysikalischer Methoden zeigen, mit welchen molekularen Hilfsmitteln das Enzym den Umbau der Phosphate aus der Quelle ins Depot realisiert.
„Dabei ist besonders interessant, dass der Aufbau der kettenförmigen Depotsubstanz und deren gleichzeitiger Transport in eine zelluläre Untereinheit mit Hilfe einer tunnelartigen Proteinstruktur erfolgt“, erklärt Professor Christian Herrmann vom Lehrstuhl Physikalische Chemie I der RUB. Das Enzym VTC ist Teil eines größeren Protein-Komplexes, der durch eine innere Membran der Zelle reicht. Seine Charakterisierung stellt einen Meilenstein für die Erforschung von ATP-abhängigen Membranprozessen dar.
Wichtige Protein-Forschung
An der Ruhr-Universität hat sich in den vergangenen Jahren eine besondere Stärke im Bereich der Protein-Forschung etabliert, die sich vor allem in der erfolgreichen Fortführung des Sonderforschungsbereichs 642 – ATP- und GTP-abhängige Membranprozesse – und der Gründung des Protein-Research Departments zeigt.
Die besondere experimentelle Ausstattung und die Erfahrung der dort aktiven Wissenschaftler schaffen die Grundlage, um Probleme der modernen Life Sciences mit der notwendigen Effizienz im internationalen, stark konkurrierenden Forschungsumfeld anzugehen und zeitnah zu lösen.
Nachwuchsforscher erfolgreich
„Besonders erfreulich ist in diesem Zusammenhang, dass der Biochemiker Mark Wehner als Stipendiat aus der Research School der RUB den maßgeblichen Beitrag auf der Bochumer Seite geliefert hat und damit das Konzept der Förderung von wissenschaftlichem Nachwuchs im Rahmen der Exzellenzinitiative bestätigt wird“, unterstreicht Herrmann.
(idw – Ruhr-Universität Bochum, 29.04.2009 – DLO)