Wenn Zellen hungern, laufen Alterungsprozesse langsamer ab und die Lebensspanne von Organismen verlängert sich. Als mitverantwortlich für diese Mechanismen werden schon lange Proteine der Sirtuin-Familie angesehen. Die genauen Aufgaben ihrer sieben Mitglieder bei Säugetieren waren allerdings ungeklärt – bis jetzt.
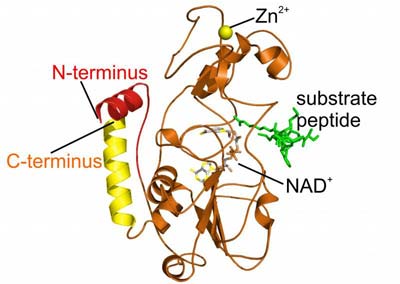
Denn erstes Licht ins Dunkel bringen nun neue Ergebnisse von Bochumer und Dortmunder Proteinforschern um Juniorprofessor Dr. Clemens Steegborn vom Institut für Physiologische Chemie der Ruhr-Universität Bochum (RUB). Sie stellen erste Funktionen der beiden menschlichen Sirtuine Sirt3 und Sirt5, die sich in den Mitochondrien, den Energie liefernden Zellkraftwerken aufhalten, in der aktuellen Ausgabe des „Journal of Molecular Biology“ vor.
Einfluss auf das zelluläre Selbstmordprogramm
Mitochondrien sind in der Zelle für die Bereitstellung von Energie durch Verwertung von Nahrungsmolekülen verantwortlich. Daher liegt es nahe, dass dort lokalisierte Sirtuine am lebensverlängerten Effekt von Nahrungsmangel mitwirken.
Die Forscher fanden allerdings heraus, dass Sirt5 sich nicht nur im Innern der Mitochondrien befindet, sondern auch im so genannten Intermembranraum zwischen äußerer und innerer Membran der Mitochondrien. Dort kann es das Protein Cytochrom c modifizieren, das sowohl bei der Energiegewinnung als auch beim zellulären Selbstmordprogramm – Apoptose -, der Reaktion auf extremen zellulären Stress, eine zentrale Rolle spielt.
„Eine Störung der Apoptose könnte die vermutete Rolle von Sirt5 bei bestimmten Krebserkrankungen erklären“, so Steegborn, „aber die genaue Funktion von Sirt5 und der Modifikation von Cytochrom c konnten noch nicht endgültig geklärt werden.“
Alternative Energiequellen nutzen
Für Sirt3 fanden die Wissenschaftler dagegen eine klar definierte Funktion. Sie konnten zeigen, dass Sirt3 zwei zentrale Stoffwechselenzyme verändert und sie dadurch aktiviert. Diese Aktivierung ermöglicht es der Zelle, bei Mangel an herkömmlichen Nährstoffen andere Energiequellen zu verwenden und diese effizient zu nutzen.
Sirt3 aktiviert dabei spezielle Formen dieser Enzyme, die gleichzeitig NADPH bilden, welches für die Regeneration zellulärer Anti-Stress-Systeme benötigt wird. Das erklärt, wie die bei Nahrungsmangel erhöhte Sirt3-Aktivität zu einer verlängerten Lebensspanne beitragen kann.
Fernziel: Gesundes Altern
Verschiedene Forschergruppen konnten in Modellorganismen zeigen, dass eine Erhöhung von Sirtuinaktivität deren Lebensspanne verlängern kann. Die Situation im Menschen ist allerdings komplexer, da hier sieben verschiedene Sirtuine an verschiedenen Orten in der Zelle und jeweils mit spezifischen Funktionen zu finden sind.
Die aktuellen Ergebnisse der Bochumer und Dortmunder Forscher sind ein erster Schritt zum Verständnis dieser Prozesse. Ein detailliertes Wissen über die spezifischen Funktionen ist Voraussetzung, um für eine gewünschte therapeutische Wirkung das richtige Sirtuin als Zielmolekül zu verwenden.
„Dadurch wird sich vermutlich kein lebensverlängerndes Elixir finden“, schätzt Steegborn, „aber wir hoffen, durch diese Arbeiten Wirkstoffe zu erhalten, mit denen altersbedingte Erkrankungen behandelt werden können und die somit ein ‚gesundes Altern‘ ermöglichen.“
(idw – Ruhr-Universität Bochum, 14.10.2008 – DLO)