Wachstumsprozesse in lebenden Zellen werden durch die Interaktion des Proteins Ras mit dem GAP-Protein gesteuert – Störungen in diesem Prozess etwa durch Mutationen im Ras-Protein können zur Entstehung von Krebs beitragen. Forscher haben nun die katalytischen Schritte der Protein-Protein-Interaktion zwischen Ras und GAP im Detail aufgelöst.
Wie die Wissenschaftler um Professor Klaus Gerwert und Carsten Kötting von der Ruhr-Universität Bochum und Professor Alfred Wittinghofer vom Max-Planck-Institut für Molekulare Physiologie in Dortmund in den Proceedings of the National Academy of Sciences (PNAS) berichten, entdeckten sie dabei auch die entscheidende Rolle proteingebundener Wassermoleküle.
In Krebszellen findet man veränderte Ras-Proteine. Diese onkogen mutierten Ras-Proteine können nicht mehr durch das GAP-Protein abgeschaltet werden, so dass die Wachstumsprozesse außer Kontrolle geraten. Die Zellen wachsen ungebremst und schließlich entsteht ein Tumor. Ein Verständnis des Abschaltmechanismus auf der atomaren Ebene ist eine wichtige Voraussetzung dafür, gezielt nach kleinen Molekülen forschen zu können, mit denen man die Störung des Abschaltens in so genannten molekularen Therapieansätzen beheben kann.
Protein-Katalyse beobachten
Nachdem der Konstruktionsplan für die Lebensprozesse, das Genom, entschlüsselt ist, wollen Forscher jetzt herausfinden, wie die einzelnen Bauteile in der lebenden Zelle miteinander interagieren. Bei vielen Prozessen innerhalb von Zellen finden sich so genannten G-Proteine, zu denen auch Ras gehört, als wichtige regulierende Module, die Prozesse an- und abschalten können. Dabei zeigt sich, dass beim Abschalten der G-Proteine der „Arginin-Finger“ der herunter regulierenden GAP-Proteine eine katalytische Rolle spielt.
Wittinghofer hat die wichtige Rolle des von ihm benannten „Arginin- Fingers“ für die Ras-Katalyse entdeckt. Aufbauend auf seinen Arbeiten konnten Kötting und Gerwert jetzt die einzelnen Schritte dieser Interaktion auflösen. Insbesondere konnten sie die Bewegung des entscheidenden „Arginin-Fingers“ direkt beobachten.
„Arginin-Finger“ drückt Wassermoleküle aus der Tasche
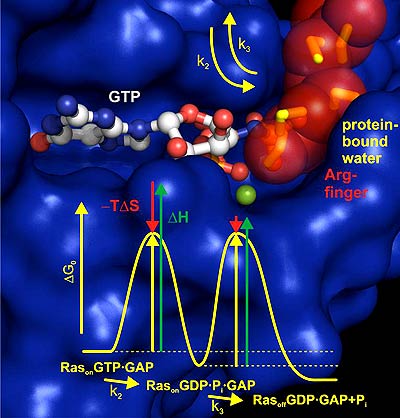
Messungen mit der zeitaufgelösten FTIR-Spektroskopie, trFTIR, zeigen, wie der positiv geladene „Arginin-Finger“ in die negativ geladene GTP-Bindetasche des Ras-Proteins gezogen wird und dabei proteingebundene Wassermoleküle aus der engen Bindetasche drückt. Die Rolle der proteingebundenen und dann freigesetzten Wassermoleküle in einer Protein-Protein-Wechselwirkung konnte zum ersten Mal detailliert aufgeklärt werden und scheint auch für andere Protein-Protein-Wechselwirkungen exemplarisch zu sein, insbesondere bei der GTP- und ATP-Hydrolyse.
„Dies ist ein wichtiger Schritt zu einem besseren Verständnis der Rolle der Wassermoleküle für die Protein-Proteinwechselwirkung“, folgert deshalb Gerwert.
trFTIR löst Proteininteraktion auf
Die vibrationsspektroskopische Methode trFTIR war entscheidend für die Entdeckung. Gerwert konnte mit dieser mehrfach preisgekrönten und zuletzt mit dem Innovationspreis Ruhr gewürdigten Methode bereits die Reaktionsmechanismen von einigen Membran-Proteinen aufklären.
Die aktuelle Studie zeigt, dass auch Protein-Protein-Interaktionen räumlich und zeitlich mit höchstmöglicher Auflösung identifiziert und so das komplexe dynamische Wechselspiel der Proteine auf atomarer Ebene bestimmt werden können.
(idw – Ruhr-Universität Bochum, 28.04.2008 – DLO)