Bei der Protein-Synthese wird der genetische Code in eine Kette von Aminosäuren übersetzt, die sich dann zu der dreidimensionalen Struktur eines Proteins faltet. Ist die Protein-Biosynthese gestört, gerät die Maschinerie des Lebens ins Stocken. Daher ist sie ein beliebtes Angriffsziel anti-mikrobieller Wirkstoffe, die unerwünschte Krankheitserreger abtöten sollen. Und so greifen die meisten der neu entwickelten Antibiotika genau in diesen komplexen Prozess am Ribosom ein. Wissenschaftlern ist es nun erstmals gelungen, das Andocken von Antibiotika an einem neuen Ort der bakteriellen Proteinfabrik, dem Ribosom, in drei Dimensionen sichtbar zu machen.
Dabei haben die Forscher der Universität Frankfurt am Main neue Erkenntnisse über den Prozess der Protein-Biosynthese gewonnen, über die sie in der aktuellen Ausgabe der Fachzeitschrift Molecular Cell berichten.
Das Ribosom setzt sich zu Beginn der Protein-Biosynthese aus zwei Untereinheiten zusammen, einer kleinen, die für die Übersetzung des genetischen Codes verantwortlich ist, und einer großen, an welcher die Aminosäuren zu einer Kette verknüpft werden. Strukturelle Erkenntnisse über Bindungsstellen und Funktion von Antibiotika an der großen Untereinheit bezogen sich bisher alle auf den Ort, an dem das neu entstehende Protein zusammengestellt wird (Peptidyl-Transferase-Zentrum).
Wichtige Erkenntnisse für die Entwicklung neuer Antibiotika
Wissenschaftlern um Professor Paola Fucini vom Frankfurter Exzellenzcluster Makromolekulare Komplexe ist es jetzt mittels Röntgenstrukturanalyse gelungen, die Störung einer weiteren wichtigen Funktionsregion (GTPase Associated Region) durch die Einwirkung von drei Thiopeptid- Antibiotika auf struktureller Ebene darzustellen. Dabei ergaben sich nicht nur wichtige Erkenntnisse für die Entwicklung neuer, wirksamer Antibiotika, sondern es wurde auch ein weiteres Puzzleteil zur genauen Kenntnis des Ablaufs der Proteinsynthese gefunden.
Die Proteinbiosynthese im Ribosom ähnelt dem Knüpfen einer langen Proteinkette an einem Fließband. Entscheidend für einen störungsfreien Ablauf ist die korrekte Positionierung sowie das geordnete Weiterrücken der transfer-RNA (tRNA) auf dem Fließband, auch Translokation genannt. Die tRNA liest sozusagen an einem Ende den Bauplan für das zu synthetisierende Protein und stellt am anderen Ende die entsprechende Aminosäure bereit. Die dafür notwendige Energie wird von so genannten Elongations-Faktoren bereitgestellt, die an die GTPase Associated Region im Ribosom andocken.
Antibiotika stören Proteinbiosynthese
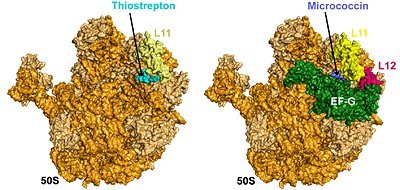
Wie stören Antibiotika diesen Prozess? Das Forscherteam fand heraus, dass sich zwei der untersuchten Antibiotika – Thiostrepton und Nosiheptide – mit der Kontaktregion des Elongations-Faktors-G (EF-G) überlagern und damit den Energie-Nachschub blockieren. Darüber hinaus bewirken sie eine Konformationsänderung der molekularen Umgebung, so dass die korrekte Bindung und Funktion dieses Elongations-Faktors nicht mehr möglich ist. Damit wird die korrekte Positionierung der t-RNA verhindert, was letztendlich zum Stillstand der Proteinbiosynthese auf dem ribosonalen Fließband führt.
Micrococcin, das dritte untersuchte Antibiotikum, bewirkt dagegen fast das genaue Gegenteil: Es führt zu einer Konformationsänderung, die die Bindung eines relativ flexibel bewegbaren ribosomalen Proteins unterstützt und damit die optimale Kontaktumgebung für den Elongatonsfaktor schafft. Dies konnte im Rahmen der Forschungskooperation, an der auch das Max-Planck-Institut für Molekulare Genetik und die Charité in Berlin sowie die Universitäten in München und Marburg beteiligt waren, zum ersten Mal auf struktureller Ebene dargestellt werden.
Schon bald neue Medikamente?
Die antimikrobielle Wirkung des Antibiotikums besteht in diesem Fall darin, ausschließlich diesen einen Zustand auszubilden, so dass die relativ variable Region für die anderen Zustände sowie andere Elongations-Faktoren blockiert sind. Somit kommt auch hierbei die Proteinbiosynthese zum Stillstand.
Obwohl die hier untersuchten Antibiotika nicht auf menschliche oder tierische Zellen wirken, geht aus aktuellen Untersuchungen hervor, dass sie auch Einfluss auf das Wachstum der Malaria Parasiten haben. Mit Sicherheit können die gewonnenen strukturellen Bindungsinformationen gezielt verwendet werden, um neue Medikamente zu erzeugen.
(idw – Universität Frankfurt (Main), 14.04.2008 – DLO)