Winzige Kanäle in den Zellwänden der Nervenzellen spielen eine Schlüsselrolle in der elektrischen Signalübertragung in Nervenzellen. Bisher war die Struktur dieser von Botenstoffen gsteuerten Ionenkanäle jedoch nur teilweise bekannt. Erst jetzt gelang es Forschern, die detaillierte Struktur von solchen Neurotransmitter-Rezeptoren zu entschlüsseln. Ihre Ergebnisse sind jetzt in der Online-Ausgabe des Wissenschaftsmagazins „Nature“ erschienen.
Vom Denken bis zur Bewegung wird unser Körper durch Elektrizität gesteuert. Grundlage für solche elektrischen Prozesse ist der kontrollierte Fluss von geladenen Teilchen, den Ionen, durch die Wände der Zellen. Da die Zellmembran für Ionen undurchlässig ist, braucht es so genannte Ionenkanäle. Diese sind selektiv und erlauben nur bestimmten Ionen den Durchfluss durch die Membran und anderen nicht. Die aus Proteinen bestehenden Kanäle reagieren auf Signale von Botenstoffen, den Neurotransmittern, und öffenen ode schließen sich daraufhin.
Je nachdem, welche Ionen sie durchlassen, aktivieren oder unterdrücken diese Rezeptoren elektrische Signale. Die Vertreter dieser Familie, die aktivierende Acetylcholin- und Serotonin-Rezeptoren und inhibierende Gaba- und Glycin-Rezeptoren, sind wichtige Angriffspunkte für Medikamente, denn ihre Fehlfunktion ist die häufig Ursache für neurologische Krankheiten. Obwohl verschiedene Rezeptoren während der letzten Jahrzehnte im Brennpunkt der biochemischen Forschung gestanden sind, waren bisher noch keine detaillierten Strukturen dieser wichtigen Proteinklasse bekannt.
Dieser Durchbruch wurde jetzt von der Arbeitsgruppe von Professor Raimund Dutzler am Biochemischen Institut der Universität Zürich erzielt. Für ihre Studien haben sich die Wissenschafter nahe bakterielle Verwandte von Neurotransmitter-Rezeptoren zu Nutze gemacht. In aufwendigen experimentellen Versuchen erzeugten sie das Protein in Bakterien, isoliert es und brachten es zur
Kristallisation, um so den Aufbau studieren zu können. Mit Hilfe der Röntgenstrukturanalyse konnten die Forschenden dann die Raumstruktur des Ionenkanals aufklären.
Fünf Ketten und eine Andockstelle
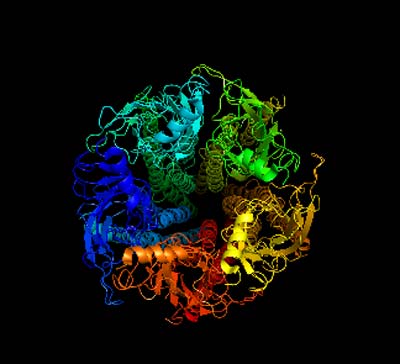
Die Struktur zeigt ein Protein, das sehr ähnlich wie die humanen Rezeptoren aufgebaut ist. Aus diesem Grund dient der kompaktere bakterielle Rezeptor als wichtiges Modellsystem, um die grundlegenden Funktionsmechanismen wie das kontrollierte Öffnen und Schliessen des Kanals und seine Präferenz für
bestimmte Ionen zu untersuchen.
Der Kanal wird aus fünf gleichen Proteinketten gebildet. Er besteht aus zwei Teilen, einer Bindungsdomäne, die aus der Zellmembran herausragt und den Neurotransmitter bindet, und einem engen Kanal, der in der Membran sitzt und den Ionenfluss reguliert. Der Kanal der untersuchten Struktur ist geschlossen, wie der offene Kanal aussieht, ist im Moment noch nicht bekannt.
Laut Dutzler bildet die Struktur einen ersten wichtigen Teil eines Puzzles. Doch es benötigt weitere Experimente, um zu einem kompletten Bild zu gelangen, einem Bild, das am Ende den detaillierten Mechanismus dieses wichtigen physiologischen Prozesses zeigt und das zur Entwicklung neuer Medikamente beitragen kann.
(Universität Zürich, 06.03.2008 – NPO)