Wie der Transport von Schlüsselproteinen der Immunantwort zu ihrem „Arbeitsplatz“ an der Zelloberfläche reguliert wird, hat ein internationales Wissenschaftlerteam jetzt erstmals gezeigt. Die Forscher berichten über ihre Ergebnisse in der aktuellen Online-Ausgabe des Journal of Biological Chemistry.
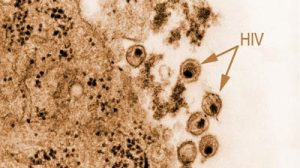
Um eine Virusinfektion erfolgreich zu bekämpfen, muss das menschliche Immunsystem infizierte Zellen aufspüren. Im Allgemeinen vermehren sich Viren aber im Zellinneren und sind so vor den im Blut zirkulierenden Antikörpern und den Immunzellen, den Lymphozyten, verborgen. Das Aufspüren der verborgenen Viren ist die Aufgabe von Transportproteinen, so genannten MHC (Major Histocompatibility Complex oder Haupt-Histokompatibilitätskomplex)-Klasse-I-Molekülen: Sie bringen Proteinfragmente – Peptide – aus dem Zellinneren an die Oberfläche, wo sie dann von den Lymphozyten als Virenbestandteile erkannt werden können. Die virusinfizierte Zelle wird dann beseitigt.
Bislang ungelöst war die Frage, wie der Transport der MHC-Klasse-I-Moleküle an die Zelloberfläche reguliert wird und wie der Transport ausgelöst wird, wenn die Transportmoleküle „Abfall-Peptide“ aufgenommen haben.
„Qualitätskontrolle“ am Golgi-Apparat
Professor Sebastian Springer und seine Arbeitsgruppe an der Jacobs University Bremen konnten nun zusammen mit Rainer Duden von der Royal Holloway University London zeigen, dass die MHC-Klasse-I-Moleküle durch einen Mechanismus reguliert werden, der beispielsweise auch den Transport von Hormonen oder Zelloberflächenrezeptoren aus dem Zellinneren steuert: Die MHC-Klasse-I-Moleküle verlassen in Transportbläschen, den Vesikeln, den Ort ihrer Entstehung innerhalb der Zelle, das Endoplasmatische Retikulum (ER).
Unabhängig von ihrem Beladungszustand mit Peptiden werden sie zunächst an eine Zwischenstation, den Golgi-Apparat, transportiert, wo sie einer „Qualitätskontrolle“ unterworfen werden. Fehlt ein gebundenes Peptidfragment und dem MHC- Klasse-I-Molekül daher die strukturelle Festigkeit, so werden sie wieder zurück ins ER geschickt und bei der nächsten Runde aufs Neue überprüft. Erst mit fest gebundenem Peptid können sie den Weg an die Zelloberfläche antreten. Die gängige Lehrmeinung war bisher, dass MHC-Klasse-I-Moleküle das ER gar nicht verlassen können, bis sie Peptide gebunden haben, weshalb die Kontrolle ihres Beladungszustandes bislang völlig unverstanden war.
Hamster helfen Forschern
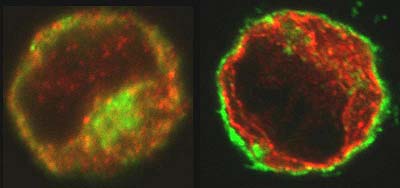
Für ihre Untersuchungen verwendeten die Wissenschaftler Zellkulturen von menschlichen und Hamster-Lymphozyten. Neben der fluoreszenzmikroskopischen Untersuchung einzelner Zellen zur Verteilung unbeladener MHC-Klasse-I-Moleküle setzten die Forscher eine neuartige Methode zur In-vitro-Isolierung von intrazellulären Transportvesikeln ein, die sie auf den Peptid-Beladungszustand der der darin enthaltenen MHC-Klasse-I-Moleküle überprüften.
„Die antivirale Immunantwort wird durch einen Mechanismus kontrolliert, der für präziseste Kontrolle und größtmögliche Effizienz sorgt. Unsere Arbeiten zum besseren Verständnis dieses Mechanismus zielt letztendlich auf die Verbesserung von Impfstoffen und die therapeutische Unterstützung des Immunsystems“, kommentiert der Jacobs-Wissenschaftler Springer den Forschungserfolg.
(idw – Jacobs University Bremen, 19.10.2007 – DLO)