Weiße Blutkörperchen, Leukozyten, zirkulieren mit dem Blut durch den ganzen Körper. Sie verlassen die Blutbahn nur dort, wo sie für die Immunabwehr benötigt werden, wie zum Beispiel in der Nähe von Entzündungsherden. Wie dies genau geschieht, haben jetzt Max-Plack-Forscher herausgefunden.
Die Leukozyten „rollen“ an den Wänden der Blutgefäße entlang, um sie systematisch nach Stopsignalen abzusuchen. Der gleiche Mechanismus wird auch von Stamm- und Krebszellen benutzt, wenn sie sich im Körper ausbreiten. Zusammen mit Kollegen vom Weizmann-Institut in Israel ist es jetzt Ulrich Schwarz vom Potsdamer Max-Planck-Institut für Kolloid- und Grenzflächenforschung gelungen, mit Hilfe von Flusskammer-Experimenten und Computersimulationen zu beschreiben, wie die „rollende Adhäsion“ der Leukozyten im Detail eingeleitet wird. Bei niedrigen Durchflussraten beobachteten die Forscher nur kurzlebige Einzelbindungen zwischen Leukozyten und Umgebung, während sie oberhalb einer kritischen Durchflussrate die Bildung von Mehrfachbindungen mit schneller Rückbindungsrate fanden, die zu einer dramatischen Stabilisierung der rollenden Adhäsion führt. Dieser Mechanismus trägt dazu bei, dass die Adhäsion von Leukozyten außerhalb des Blutstroms unterdrückt und nur in den Blutgefäßen eingeleitet wird.
„Postleitzahlensystem“ steuert Blutkörperchen
Leukozyten sind die „Wächter“ des Immunsystems und für die Abwehr von körperfremden Substanzen verantwortlich. In jeder Minute dringen in unserem Körper Hunderte Millionen von weißen Blutkörperchen aus den Blutgefäßen in das umgebende Gewebe, um dieses nach Verletzungen und Entzündungen abzusuchen. Die Logistik dieser Transportströme wird durch ein kompliziertes „Postleitzahlensystem“ gesteuert, das dafür sorgt, dass die richtigen Unterarten von weißen Blutkörperchen die Blutbahn genau am richtigen Ort verlassen. Dieses Postleitzahlensystem beruht auf einer Vielzahl von Botenstoffen und Adhäsionsmolekülen, die sich komplementär sowohl auf den Leukozyten als auch an den Wänden der Blutgefäße befinden.
Versagt das Postleitzahlensystem, führt das zu Krankheiten wie der Leukozyten-Adhäsions-Defizienz, bei der es weißen Blutkörperchen wegen eines Defekt in einem bestimmten Adhäsionsmolekül nicht mehr gelingt, die Blutbahn zu verlassen. Bei betroffenen Patienten bleiben offene Wunden ohne weiße Blutkörperchen, was zu erhöhter Anfälligkeit gegenüber Infektionen führt. Das Postleitzahlensystem der weißen Blutkörperchen wird aber auch von metastasierenden Krebszellen verwendet, die sich auf diese Weise über die Blutbahn im ganzen Körper ausbreiten können.
„Rollende Adhäsion“ als Stoppsignal
Beim Verlassen der Blutbahn stehen die weißen Blutkörperchen vor einem offensichtlichen Problem: Selbst wenn an den Wänden der Blutgefäße die richtigen Informationen für den Bedarf an weißen Blutkörperchen vorhanden sind, ist es für die Leukozyten schwierig, diese wahrzunehmen, da sowohl sie selbst als auch eventuell ausgeschüttete Botenstoffe sehr schnell im Blutstrom davongetragen werden. Im Prinzip könnten starke Adhäsionsmoleküle die weißen Blutkörperchen – wie ein starker Magnet – aus dem Blutstrom fischen, aber dies würde nicht nur zu einer starken Beeinträchtigung des Blutstroms selbst führen, sondern auch dazu, dass die Zellen nur jene Signale wahrnehmen, die genau an der Adhäsionsstelle liegen.
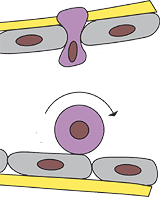
Hier hat die Natur eine trickreiche Lösung entwickelt, nämlich die so genannte „rollende Adhäsion“: Durch die Verwendung von schwachen Adhäsionsmolekülen kommt es nur zur kurzzeitigen Bindung der weißen Blutkörperchen an die Wände der Blutgefäße. Da der Blutstrom dabei kontinuierlich an den Leukozyten zieht, entstehen neue Kontakte nach der Aufbrechen der kurzlebigen Bindungen immer nur stromabwärts. Auf diese Weise beginnen die Zellen, an den Wänden der Blutgefäße zu rollen, ähnlich wie Kiesel in einem Flussbett. Die rollende Adhäsion erlaubt es den weißen Blutkörperchen, die Wände der Blutgefäße auf Signale abzusuchen, ohne dabei den Blutstrom selbst zu sehr zu stören. Sind solche Signale tatsächlich vorhanden, werden die starken Adhäsionsmoleküle in den Blutzellen aktiviert: Die rollende Adhäsion kommt zu ihrem Ende und die weißen Blutkörperchen quetschen sich durch die Zellen der Blutgefäße in das umliegende Gewebe.
Mehrfachbindungen als Schlüssel
Dr. Ulrich Schwarz vom Potsdamer Max-Planck-Institut für Kolloid- und Grenzflächenforschung und Prof. Ronen Alon von der Abteilung für Immunologie am Weizmann-Institut, Israel, konnten jetzt nachweisen, dass ein entscheidender Aspekt der rollenden Adhäsion von weißen Blutkörperchen über die schnelle Stabilisierung von Mehrfachbindungen vermittelt wird.
Ein Hauptergebnis dieser Arbeiten ist eine neue Erklärung, warum die rollende Adhäsion erst oberhalb einer bestimmten Durchflussrate einsetzt. Dieser Mechanismus dürfte in unserem Körper sehr wichtig sein, um zu verhindern, dass Leukozyten außerhalb des Blutstroms adhärieren. Tatsächlich wird ihre Adhäsion im wesentlichen nur in den Blutgefäßen, also bei ausreichender Durchflussrate benötigt. Obwohl die Modellierung von Schwarz und Alon noch nicht die gesamte Komplexität des Vorgangs erfasst, beschreibt und erklärt sie doch einen bisher unbekannten und sehr wesentlichen Schritt in der rollenden Adhäsion – die anfängliche Stabilisierung durch Doppelbindungen. Damit haben die Wissenschaftler neue Möglichkeiten aufgezeigt, wie man einen für das Immunsystem sehr wichtigen Prozess in Zukunft besser kontrollieren kann.
(MPG, 23.04.2004 – NPO)