Der Reigen der Nobelpreise hat begonnen. Heute um 11.00 Uhr verkündete das Nobel-Komitee die Träger des Medizin-Nobelpreises 2007. Ausgezeichnet werden drei Genforscher, die US-Amerikaner Mario Capecchi und Oliver Smithies sowie an den Briten Martin J. Evans. Sie entwickelten eine Technik, mit der bei Mäusen gezielt einzelne Gene ausgeschaltet werden können und so deren Funktion untersucht werden kann.
Die als “Gene targeting” bezeichnete Methode zählt heute zu einem der wichtigsten Werkzeuge der modernen Biotechnologie. Sie wird sowohl in der Grundlagenforschung als auch bei der gezielten Suche nach neuen Wirkstoffen eingesetzt. Mehr als zehntausend Gene, und damit nahezu die Hälfte des gesamten Säugetiergenoms, konnten damit bereits „ausgeschaltet“ und ihre Funktionen untersucht werden. Mehr als 500 Mausmodelle menschlicher Krankheiten wurden so geschaffen.
Ansatzpunkt: Genaustausch zwischen Chromosomen
Basis des gezielten Gen-Ausschaltens ist die Tatsache, dass fast alle Gene in unseren Zellen immer in zwei Kopien vorliegen, auf jedem Chromosom eines Chromosomen-Paares eine. Der Austausch von DNA-Sequenzen zwischen den beiden Chromosomen, die so genannte homologe Rekombination, trägt zur genetischen Variation in einer Population bei.
Die Wissenschaftler Mario Capecchi und Oliver Smithies kamen nun beide auf die Idee, diese homologe Rekombination zu nutzen, um gezielt Gene von Säugetieren zu beeinflussen. Capecchi demonstrierte in Versuchen, dass diese Form der Rekombination auch zwischen einer künstlich in das Genom eingeschleusten DNA-Sequenz und den Chromosomen funktioniert und zeigte, dass auf diese Weise sogar defekte Gene gezielt ersetzt werden können.
Smithies ging von Versuchen aus, mutierte Zellen im menschlichen Knochenmark zu reparieren. Dabei belegte er, dass der Genaustausch durch homologe Rekombination unabhängig vom Aktivitätszustand der Gene stattfindet. Er funktioniert sowohl bei aktiven als auch bei ruhenden Genen.
Entdeckung der embryonalen Stammzellen
Mit ihren Entdeckungen hatten Capecchi und Smithies zwar einen Weg geebnet, um Gene gezielt auszutauschen. Was ihnen aber noch fehlte, war eine Möglichkeit, ganze Organismen zu züchten, die diese veränderten Gene in allen ihren Zellen und Geweben besaßen. Und hier kam der Dritte im Bunde, Martin Evans ins Spiel. Er hatte mit an Krebsstammzellen aus Mäuseembryonen gearbeitet. Diese stammen zwar aus Tumoren, können aber, wie andere embryonale Stammzellen auch, prinzipiell noch alle Zelltypen erzeugen.
Evans schwebte vor, diese Zellen als Vehikel zu nutzen, um genetisches Material in die Keimbahn von Mäusen einzuschleusen und damit die künstlich erzeugten Genveränderungen an die nächste Generation weiterzugeben. doch zunächst scheiterte er, da die Chromosomen der Krebsstammzellen Anomalitäten enthielten, die die Entstehung gesunder Keimzellen verhinderte. Daraufhin entdeckte er, dass es in den frühen Stadien von Mäuseembryonen Zellen gab, die normale Chromosomen besaßen, nicht aus Tumoren stammten und trotzdem noch alle Zelltypen bilden konnten – die embryonalen Stammzellen.
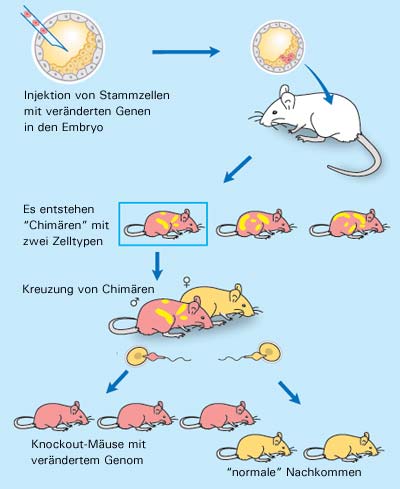
Aber konnte er mit ihrer Hilfe die Keimbahn der Mäuse genetisch verändern? Um dies zu testen injizierte er Embryos eines Mäusestamms embryonale Stammzellen eines anderen Stamms. Es entstanden so genannte „Mosaik-Embryos“, die Zellen beider Stämme enthielten. Die entstehenden Mäuse kreuzte Evans miteinander und untersuchte, ob sich die Gene aus den künstlich eingeschleusten Genen auch noch in deren Nachwuchs fanden. Als dies tatsächlich der Fall war, hatte Evans damit bewiesen, dass er mithilfe der injizierten Stammzellen fremde Gene in die Keimbahn und damit dauerhaft in ihre Erbinformation eingebracht hatte.
Die erste Knockout-Maus
1986 waren so alle Voraussetzungen für die Methode des „gene targeting“ erfüllt: Capecchi und Smithies konnten gezielt Gene mithilfe der homologen Rekombination ansteuern und Evans wusste, wie man Erbinformation in die Keimbahn eines Organismus einschleust. Beide Methoden kombiniert führten 1989 schließlich zur ersten „Knockout-Maus“, einem Mäusestamm, bei dem ein bestimmte Gen dauerhaft ausgeschaltet war. Seither ist die Anzahl solcher Stämme exponentiell gestiegen.
Mit ihrer Hilfe wurden die Gene dingfest gemacht, die Erbkrankheiten wie Mukoviszidose oder die Thalassämie hervorrufen, aber auch diejenigen, die die Herausbildung unserer Körperform während der Embryonalentwicklung steuern. Ohne die Knockout-Mäuse wäre auch die Forschung an Möglichkeiten der Gentherapie kaum denkbar. Kaum ein Bereich der Biomedizin und Biotechnologie kommt heute noch ohne sie aus. Und genau deshalb hat das Stockholmer Nobelkomitee den drei Forschern den Medizin-Nobelpreis verliehen.
(Nobelfoundation, 08.10.2007 – NPO)