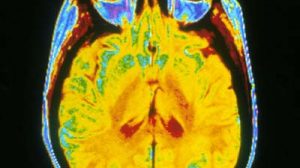
Rund eine Million Menschen leiden in Deutschland unter „Alzheimer“. Damit ist diese Krankheit die häufigste neurodegenerative Erkrankung im Alter. Welche Ursachen Alzheimer hat, ist aber noch immer weitgehend unklar. Nun jedoch sind deutsche Wissenschaftler dabei einen entscheidenden Schritt weitergekommen. Sie haben festgestellt, dass die für die Krankheit typischen Eiweiß-Plaques im Gehirn, die vorwiegend aus Abeta-Peptid bestehen, das Enzym ATP-Synthase zumindest teilweise außer Gefecht setzen. Folge: Der Energiestoffwechsel der Nervenzellen und die Synapsentätigkeit sind gestört, so die Forscher in der Fachzeitschrift „Molecular Psychiatry“.
{1r}
Neurodegenerative Krankheiten wie Alzheimer führen zum Absterben von Nervenzellen. In den Gehirnen von Alzheimer-Patienten haben Wissenschaftler eine große Zahl von Ablagerungen bei Nervenzellen nachgewiesen, die hauptsächlich aus dem so genannten Abeta-Peptid bestehen. Bei diesem handelt es sich um ein kurzes Bruchstück eines größeren Proteins. Es entsteht, wenn dieses Vorläuferprotein falsch abgebaut wird.
Neue Bindungspartner für das Abeta-Peptid
Für den Zeitpunkt des Ausbruchs und den Verlauf der Krankheit ist es entscheidend, wie viel Abeta-Peptid im Gehirn entsteht. Unbekannt ist jedoch unter anderem, inwiefern das Abeta-Peptid zum Absterben der Nervenzellen führt. Daher bemühen sich Forscher um die Identifizierung von Molekülen in den Nervenzellen, die das Abeta-Peptid binden, so dass dieses zur Erkrankung der Nervenzelle beitragen kann.
Die Wissenschaftler des Zentrums für Molekulare Neurobiologie (ZMNH) am Universitätsklinikum Hamburg-Eppendorf (UKE) fanden nun neue Bindungspartner für das Abeta-Peptid. Eines dieser Moleküle ist die ATP-Synthase. Dieses Enzym konnte bisher hauptsächlich in den Mitochondrien nachgewiesen werden, wichtigen Energielieferanten in den Zellen, deren Inaktivierung zum Zelltod führen kann. Die Forscher entdeckten aber unerwartet, dass die ATP-Synthase auch an der Zelloberfläche vorkommt – ebenso wie das Abeta-Peptid.
Bindung verhindern
Die Wissenschaftler um Professorin Dr. Melitta Schachner Camartin, schließen daraus, dass die Bindung zwischen dem Abeta-Peptid und der ATP-Synthase gleich zweifach schädlich auf die Nervenzelle wirken kann: Da die ATP-Synthase über das Zellplasma in die Mitochondrien gelangt, kann sie einerseits vom im Zellplasma vorhandenen Abeta-Peptid „abgefangen“ werden. Dadurch ist sie nicht mehr in der Lage, ihre für die Zelle lebenswichtige Funktion in den Mitochondrien wahrzunehmen. Folge: Der Energiestoffwechsel der Nervenzellen wird gestört.
In Experimenten wiesen die Forscher andererseits aber auch nach, dass die Inaktivierung der ATP-Synthase durch das Abeta-Peptid an der Zelloberfläche zu einer schwächeren Synapsentätigkeit führt: Die so genannte Langzeit-Potenzierung, ein Nachweisverfahren für die Gedächtnisleistung, wird unterdrückt.
Ließe sich verhindern, dass das Abeta-Peptid an die ATP-Synthase bindet, könnte ein weiterer Weg gefunden werden, um das Auftreten der Alzheimer-Krankheit zu verhindern oder zumindest zu verzögern, so die Wissenschaftler.
(idw – Universitätsklinikum Hamburg-Eppendorf, 02.10.2007 – DLO)