Ein kleines Zuckermolekül zeigt als Begleiter von Proteinen große Wirkung. Bemerkbar macht sich das, wenn der Zucker fehlt, wie es unter anderem bei einer seltenen Erbkrankheit der Fall ist. Bei der so genannten Leukozyten-Adhäsions-Defizienz (LAD II) sind die Zellen nicht in der Lage, Moleküle des Zuckers Fucose an Proteinen anzubringen. Die Kranken können kaum sprechen, nur unsicher gehen und bleiben in ihrem körperlichen Wachstum weit zurück. Zudem sind sie sehr anfällig für normalerweise harmlose Infektionen, die aber das Leben von LAD II-Patienten bedrohen.
{1l}
Forscher um Professor Christian Körner von der Universitätsklinik für Kinder- und Jugendmedizin Heidelberg haben nun Mäuse hergestellt, die den gleichen genetischen Defekt wie LAD-Patienten aufweisen, und zusammen mit Wissenschaftlern vom Max-Planck-Institut für molekulare Biomedizin in Münster untersucht. Anhand dieser Modellmäuse wollen die Forscher herausfinden, welche Rolle der Zucker Fucose bei der Immunabwehr und der Entwicklung des Gehirns spielt.
Jede Zelle des menschlichen Körpers stellt anhand von Erbinformationen unermüdlich Proteine her, die zum Beispiel als Zellbausteine, als Antikörper oder als Katalysatoren unterschiedliche Aufgaben erfüllen. Fertige Proteine werden zunächst an den Golgi-Apparat der Zelle übergeben, der sie sortiert, umwandelt und nach Bedarf abgibt. Ihre Wirkung erhalten zahlreiche Proteine erst im Golgi-Apparat – durch ein zusätzliches Zucker-Molekül.
Zuckeranhänge mit großer Bedeutung
„Der großen Bedeutung dieser Zucker-Anhänge wird man in den letzten Jahren immer mehr bewusst“, betont Martin Wild, der Leiter der Forschungsgruppe „Vaskuläre Glykoimmunologie“ am Max-Planck-Institut für molekulare Biomedizin, „Krankheiten wie LAD II machen jedoch deutlich, dass sie eine ganz wesentliche Rolle spielen.“ Bei LAD II-Patienten ist ein bestimmtes Protein defekt, das als Transporter für die aktivierte Form des Zuckers Fucose (GDP-Fucose) fungiert. Das führt dazu, dass Proteine im Golgi-Apparat nicht mit Fucose-Molekülen versehen werden können – mit verheerenden Folgen für die geistige und körperliche Entwicklung des Patienten.
Die genetisch veränderten Mäuse der Heidelberger Forscher ahmen genau diesen Defekt nach: „Dazu hat man ein bestimmtes Gen deaktiviert, das heißt man schleust eine Fremdsequenz in das Gen ein, so dass es nicht mehr ausgelesen werden kann“, erklärt Wild in der Fachzeitschrift Journal of Biological Chemistry. Aufgrund der Manipulation fehlt den Modellmäusen das Transporter-Protein für die aktivierte Fucose. Sie zeigen ebenso wie LAD II-Patienten Immundefekte und entwickeln sich langsamer als genetisch unveränderte Mäuse. Der Forschungsgruppe um Martin Wild eröffnet die LAD II-Modellmaus einen neuen Zugang, um Immunreaktionen zu erforschen.
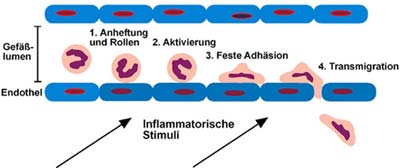
Ob die Immunabwehr eines Körpers ihre Aufgabe wirksam erfüllt, hängt vor allem davon ab, wie effizient weiße Blutkörperchen den Ort einer Entzündung erreichen. In einem gesunden Körper werden in der Umgebung einer Infektion die Wände der Blutgefäße, die Endothelzellen, aktiviert. Sie präsentieren auf ihrer Oberfläche dann spezielle Proteine, die Selektine heißen. Weiße Blutkörperchen, die an der aktivierten Gefäßwand vorbeiströmen, binden mithilfe fucosylierter Proteine – Proteine, die mit einem zusätzlichen Fucose-Molekül ausgestattet sind – an die Selektine (Adhäsion), worauf sie die Blutgefäße zum entzündeten Gewebe hin verlassen.
Mechanismus gestört
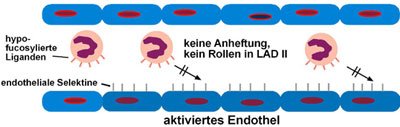
Bei LAD II-Patienten ist dieser Mechanismus gestört: Weiße Blutkörperchen – auch Leukozyten genannt – können sich mangels richtig „gezuckerter“ Proteine nicht an Blutgefäßwänden festheften und gelangen nicht zum Infektionsherd, die Immunabwehr versagt. Das Fehlen des Fucose-Transporters betrifft alle Zellen des Körpers. „Für die fehlende Immunabwehr sind aber vor allem die defekten Transporter-Proteine in den weißen Blutkörperchen verantwortlich“, erläutert Wild.
Andere Symptome des LAD II-Syndroms wie die verlangsamte mentale und körperliche Entwicklung konnten noch nicht entschlüsselt werden. „Der Mechanismus der Entwicklungsstörung kann ein ganz anderer als der beim Immundefekt sein“, so Wild. „möglicherweise ist hier nicht die Zelladhäsion gestört, sondern die Signalübertragung zwischen Zellen. Zumindest weiß man, dass die Fucose bei einem wichtigen Signalübertragungsweg eine Rolle spielt. Ob der bei LAD II gestört ist, weiß man allerdings noch nicht.“
Anhand der Modellmäuse möchten die Forscher um Körner und Sperandio in Heidelberg und Wild in Münster in Zukunft der Bedeutung der Zuckermoleküle entschlüsseln. „Wir versuchen herauszufinden, welche Rolle der Zucker Fucose bei der Entwicklung des Menschen spielt. Das er sehr wichtig ist, ist offensichtlich, da das Fehlen des Transporter-Proteins zu so gravierenden Einschnitten in der geistigen und körperlichen Entwicklung führt“, so Wild. Er wird sich am Münsteraner Max-Planck-Institut vor allem der immunologischen Seite des Problems widmen, während sich die Heidelberger Forschungsgruppe auf die neuronalen Aspekte konzentriert.
(idw – MPG, 20.04.2007 – DLO)