Die Tuberkulose fordert Jahr für Jahr zwei Millionen Todesopfer weltweit. Etwa ein Drittel der Weltbevölkerung ist infiziert. Ursachen sind eine ungenügende Versorgung mit Medikamenten, aber auch die zunehmende Häufigkeit von resistenten Stämmen des Erregers Mycobacterium tuberculosis. Wissenschaftler haben jetzt die Struktur eines Proteins aufgeklärt, welches das Bakterium braucht, um in menschlichen Zellen zu überleben. Dies eröffnet Ansatzpunkte für neue Antibiotika, wie die Forscher in den Proceedings of the National Academy of Sciences (PNAS) berichten.
Gefährlich ist der Tuberkuloseerreger, weil er sich in den Immunzellen des menschlichen Körpers versteckt hält und dort überdauert. "Sein Überleben wird durch die Aktivität von Schlüsselmolekülen gesichert", erläutert der Leiter von EMBL Hamburg, Matthias Wilmanns. "Wir untersuchen daher die Funktionen von Tuberkuloseproteinen und bestimmen ihre atomaren Strukturen, um mögliche Schwachstellen und neue Hemmstoffe zu finden." Und die Forscher der Außenstelle des Europäischen Laboratoriums für Molekularbiologie (EMBL) in Hamburg und des Max Planck Instituts für Infektionsbiologie in Berlin (MPIIB) wurden fündig:
Protein verriet sich durch erhöhte Aktivität
Eines der lebenswichtigen Proteine des Organismus ist LipB – lebenswichtig, weil es Zellmaschinerien aktiviert, die dem Bakterium als Stoffwechselmotoren dienen. Die Forschungsabteilung von Stefan Kaufmann, Direktor am MPIIB, hat sich auf die Biologie der Infektion mit M. tuberculosis und dessen Überlebensstrategien in Immunzellen spezialisiert. Dabei kamen die Forscher einer erhöhten Aktivität von LipB in akut infizierten Zellen auf die Spur, insbesondere bei Patienten, die mit Formen des Bakteriums infiziert waren, die bereits gegen zahlreiche Wirkstoffe eine Resistenz entwickelt hatten.
"In diesen Zellen beobachten wir eine im Vergleich zu anderen Zellen 70-fach erhöhte Produktion von LipB – ein deutlicher Hinweis darauf, dass das Protein an der Pathogenese beteiligt ist", erklärt Kaufmann. "Dadurch wird es zu einem besonders interessanten Angriffspunkt, wo traditionelle Wirkstoffe keine Wirkung mehr zeigen."
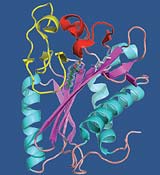
Atomare Karte der Struktur zeigt Ansatzstellen
Ein Strukturbild des Proteins – eine Art technisches Diagramm seines Bauplans – gab wichtige Hinweise auf seine Wirkungsmechanismen. Forscher Qingjun Ma aus Wilmanns' Team hat LipB gereinigt und kristallisiert. An den hochenergetischen Synchrotronstrahlungsquellen des EMBL in Hamburg auf dem Gelände des Deutschen Elektronensynchrotrons (DESY) stellte er eine atomare Karte der Struktur des Proteins her: Die Funktion des Enzyms ließ sich durch ein hoch aufgelöstes Bild des aktiven Bereichs von LipB, gebunden an einen Lipid-Hemmer, bestimmen. In Zusammenarbeit mit der Zentralen Einheit Proteomik am EMBL Heidelberg und Forschern der University of Illinois in den USA entdeckte die Forschungsgruppe aus Hamburg, wie LipB spezifische Fettsäuren an andere Proteine bindet.
"LipB liefert uns einen viel versprechenden Angriffspunkt für Medikamente", erläutert Wilmanns, "weil es einem lebenswichtigen Signalweg angehört. Im Unterschied zu anderen Lebewesen verfügt M. tuberculosis über keinerlei Ausweichmechanismen, die die Rolle von LipB übernehmen könnten. Ein Inhibitor, der den aktiven Bereich des Bakteriums blockiert, würde daher zentrale Prozesse lahm legen, ohne die das Bakterium nicht überleben oder sich vermehren könnte – eine sehr effektive Strategie für einen Wirkstoff."
Weitere Angriffsstellen gesucht
Die Wissenschaftler wollen nun nach Substanzen suchen, die diese Rolle übernehmen können. Parallel setzen sie ihre Suche nach weiteren potenziellen Zielproteinen für Medikamente fort. So konzentrieren sich Wilmanns und seine Kollegen an verschiedenen anderen Forschungseinrichtungen in ihrer Arbeit auf die Strukturen von Molekülen, die M. tuberculosis im Ruhestadium halten und als mögliche Angriffspunkte für Arzneimittel in Frage kommen.
In den letzten drei Jahren hat EMBL als Koordinator eines vom Bundesministerium für Bildung und Forschung [BMBF] geförderten "M.-tuberculosis-Strukturproteomik"- Konsortiums hoch aufgelöste Bilder von über 30 Proteinen hergestellt. "Im Kampf gegen zahlreiche andere Krankheiten hat sich die auf Strukturbildern basierende Arzneimittelforschung als großer Erfolg erwiesen. Diese Instrumente wenden wir nun auf die Tuberkulose an, eine der verheerendsten Infektionskrankheiten der Menschheit", schließt Wilmanns.
(Europäisches Laboratorium für Molekularbiologie, 31.05.2006 – NPO)