Wissenschaftler haben ein neues Instrument entwickelt und erfolgreich getestet, mit dem sie biologisches Material im Mikrometerbereich manipulieren und untersuchen können, ohne es aus seiner natürlichen Zellumgebung herauszureißen. Eingesetzt werden könnte es in der Zellbiologie, zur Herstellung von Mikroarrays oder in der Krebsforschung.
Die Forschung in Medizin und Biologie wird zunehmend durch den Einsatz von Biochips und so genannten mikrofluidischen Systemen revolutioniert, die im Mikrometerbereich operieren. Beispiele hierfür sind DNS-Chips, Mikroarrays aus Proteinen sowie „Lab-on-a-Chip“ Systeme. Obwohl nur so gross wie ein Fingernagel, bestehen diese Minilabors aus einer grossen Anzahl kleinster Testpunkte, mit denen zum Beispiel die Konzentration verschiedener Proteine in einer Zelle bestimmt werden kann. Die bestehenden Systeme weisen jedoch einige entscheidende Nachteile auf: Die Analysen leiden häufig unter der mangelnden Qualität der Testpunkte und können zudem nicht direkt an einzelnen Zellen in ihrer natürlichen Zellkulturumgebung durchgeführt werden.
„Hochdruckreiniger“ im Miniformat
Die Wissenschaftler David Juncker, Heinz Schmid und Emmanuel Delamarche vom IBM Forschungslabor Zürich haben im Rahmen eines Grundlagenforschungsprojektes eine innovative Technologie entwickelt, die diese Einschränkungen nicht hat und ein breites Spektrum neuartiger Funktionalitäten aufweist, speziell die Möglichkeit, einzelne Zellen zu manipulieren. In Anlehnung an das Rasterverfahren des Rastertunnel- und des Atomkraftmikroskops, beide von Forschern des IBM Forschungslabors Zürich entwickelt, bezeichnet die Gruppe ihre neue Methode als „mikrofluidische Sonde“ (microfluidic probe oder kurz MFP).
Das Funktionsprinzip der MFP-Sonde ist im Grunde einfach und vergleichbar mit dem eines Hochdruckreinigers: Ein Flüssigkeitsstrahl wird auf einen eng begrenzten Bereich einer Oberfläche gerichtet. Weil das Ganze aber im Mikrometerbereich stattfindet, werden nur Nanoliter der Flüssigkeit benötigt. Um zu verhindern, dass der dünne Strahl in benachbarte Bereiche fliesst, entwickelten die Forscher einen „Mikrosauger“, der direkt neben der Düsenöffnung angebracht ist. Der „Mikrosauger“ saugt den Flüssigkeitsstrahl sofort nach dessen Auftreffen auf die Oberfläche wieder ab.
Dank dieser Anordnung aus Düse und Sauger können mit der MFP-Sonde – wie mit Mikropipetten – winzige Materialproben, sogar Moleküle und einzelne Zellen einer Oberfläche entnommen oder auch hinzugefügt werden, ohne dass ein direkter Kontakt zwischen diesen „Pipetten“ und der Oberfläche statt findet. „Dieses kontaktfreie Verfahren ist von zentraler Bedeutung, denn so können wir die MFP-Sonde über eine Oberfläche führen und beliebige Stellen untersuchen,“ erklärt Emmanuel Delamarche.
Anwendung in Zellbiologie- und Krebsforschung
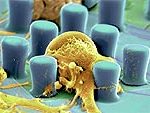
Der Einsatz der MFP-Sonde in Kombination mit einem Mikroskop erlaubt unter anderem, einzelne Zellen zu orten, die eine bestimmte Reaktion oder Symptomatik aufweisen, und sie gezielt chemischen Lösungen auszusetzen. Ebenso kann man mit dem Gerät selektiv Zellen entnehmen, um sie individuell zu untersuchen. Dass die Sonde in einer flüssigen Lösung funktioniert, ist ein grundlegender Vorteil, denn dies entspricht der natürlichen Umgebung von Biomolekülen und Zellen.
„Unsere Methode schliesst eine Lücke in der Zellbiologieforschung. Der Einfluss der extrazellulären Umgebung auf die Zellen ist von fundamentaler Bedeutung, doch bislang existierten weder praktische Verfahren noch Werkzeuge, um diese Umgebung auf der Skala der einzelnen Zelle zu gestalten,“ sagt David Juncker, der massgeblich an der Entwicklung der MFP-Sonde beteiligt war. In einem Experiment haben die IBM Forscher mit der MFP-Sonde gezielt Zellen eingefärbt und so das Wort „CELLS“ geschrieben. Es gelang ihnen auch, eine einzelne Zelle von einer Oberfläche zu entfernen, ohne die Nachbarzellen zu beschädigen.
Diese Möglichkeiten sind besonders in der Erforschung von Krebs- und Nervenzellen interessant. Ein denkbares Szenario wäre hier der Einsatz der MFP-Sonde bei der Evaluierung neuer Wirkstoffe und Medikamente. Mit Hilfe der MFP-Sonde könnte man zum Beispiel Krebszellen gezielt verschiedenen potentiellen Wirkstoffen aussetzen. Deren Wirksamkeit liesse sich genauer und differenzierter untersuchen, da man einzelne Zellen auswählen und sie mit zusätzlichen chemischen Stoffen behandeln könnte. Zudem liessen sich auch einzelne Krebszellen entfernen und für weitere Tests in einen speziellen Sensorbereich platzieren.
Mikroarrays im Schnelldurchlauf
Ein weiterer möglicher Anwendungsbereich sind Mikroarrays aus Proteinen. Mit diesen kann die Konzentration von den Proteinen in einer Zelle bestimmt werden, um eine Momentaufnahme vom Zustand der Zelle zu erhalten. MFP-Sonden können für die Herstellung von solchen Mikroarrays verwendet werden. In einer Labordemonstration stellten die Forscher mit nur einer MFP-Sonde einen Mikroarray mit mehr als Tausend Testpunkten in weniger als einer halben Stunde her.
„Wenn man die Entwicklung der Rasterkraftmikroskopie und das Spektrum ihrer Anwendungen betrachtet, kann man leicht ins Träumen geraten. Das Rastertunnel- und das Rasterkraftmikroskop erschlossen uns neue Bereiche, weil mit ihnen die Abbildung und Manipulation einzelner Atome möglich wurden. Mit der mikrofluidischen Sonde stehen uns nun ähnliche Möglichkeiten in der Zellbiologie zur Verfügung: Wir können einzelne Zellen in ihrer natürlichen Zellkulturumgebung bearbeiten,“ erklärt David Juncker und fügt hinzu: „Wir denken bereits darüber nach, wie man diese Technologie noch erweitern könnte, so dass eines Tages vielleicht sogar eine Analyse direkt im lebenden Organismus möglich sein wird. So könnte man dann beispielsweise Krebszellen markieren und gezielt entfernen oder spezifische Nervenzellen anregen.“
(IBM Research, 03.08.2005 – NPO)