Gen eingeschleust: Forscher haben die Genschere CRISPR/Cas9 erstmals genutzt, um Rinder resistenter gegenüber der Rindertuberkulose zu machen. Sie schleusten dafür in Zellen ein Schutzgen gegen die Tuberkulose-Infektion ein. Allerdings: Von 173 manipulierten Zellen entwickelten sich nur elf zu lebensfähigen Kälbern. Zudem funktioniert das Ganze nur in Kombination mit dem Klonen.
Die Genschere CRISPR/Cas9 gilt als das vielversprechendste Werkzeug der modernen Gentechnik. Denn mit ihr lassen sich Gene und Genabschnitte punktgenau ins Erbgut einschleusen und so Genfehler korrigieren. Forschern gelang es damit bereits, die Sichelzellen-Anämie bei Blutzellen zu reparieren, bei Mäusen gelang die Therapie der Duchenne Muskeldystrophie. In China haben Wissenschaftler bereits erste Genabschnitte in menschliche Embryonen eingeschleust – ein hoch umstrittener Eingriff in die menschliche Keimbahn.
Genschere treffgenauer gemacht
Allerdings: Auch CRISPR/Cas9 ist nicht unfehlbar. Manchmal treten auch bei der neuen Genschere sogenannte Off-Target-Effekte auf, indem Genteile in unerwünschten Organen oder an falschen Stellen der DNA eingebaut werden. Gleichzeitig können auch zelleigene DNA-Reparaturmechanismen dazu führen, dass eingeschleuste Gene nachträglich verändert oder beseitigt werden.
Jetzt haben Forscher um Yong Zhang von der Nordwest A&F Universität in Yangling eine Variante der Genschere entwickelt, die zielgenauer und effektiver arbeitet als bisherige Versionen. Sie erreichten dies, indem sie das Cas9-Enzym durch die Cas9-Nickase (Cas9n) ersetzten. Wie gut ihre Genscheren-Variante funktioniert, zeigen die Wissenschaftler in einer praktischen Anwendung: Erstmals haben sie CRISPR/Cas9 bei Rindern eingesetzt und diese mit einem Resistenzgen gegen die Rindertuberkulose ausgestattetet.
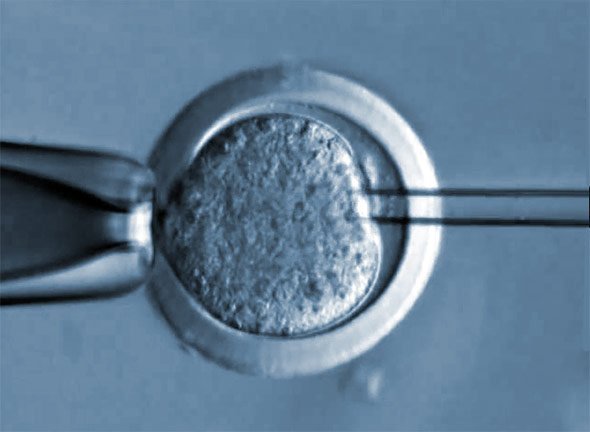
Elf Kälber aus 173 Zellen
Für ihre Studie nutzten die Forscher aus Rinderföten isolierten Bindegewebszellen. In deren Erbgut schleusten sie mit Hilfe ihrer Genschere das Resistenzgen NRAMP1 ein. In Vorversuchen hatten die Forscher geklärt, welche Stelle im Erbgut dafür am günstigsten ist. Die Kerne dieser genveränderten Zellen pflanzten die Forscher in die Hülle einer entkernten Rindereizelle. Durch diesen somatischen Kerntransfer entstand ein Rinderembryo – er wurde im Prinzip aus der manipulierten Bindegewebszelle geklont.
Die Wissenschaftler setzten 173 dieser geklonten Embryonen Leihmutter-Kühen ein, davon wurden elf Kälber geboren und überlebten. Wie Untersuchungen ergaben, war das Resistenzgen in den Zielzellen dieser Kälber enthalten, nicht aber in unerwünschten Geweben oder Organen. „Unsere Studie demonstriert damit erstmals, dass das CRISPR/Cas9n-System genutzt werden kann, um ohne unerwünschte Off-Target-Effekte transgene Nutztiere zu produzieren“, sagt Zhang.
Vor Infektion geschützt
Durch einen Infektionstest prüften die Wissenschaftler anschließend die Wirkung des neuen Resistenzgens: Sie verabreichten sechs genmanipulierten Kälber und sechs Kontrolltieren jeweils eine Dosis des Tuberkulose-Erregers Mycobacterium bovis in die Lunge. Über Blutproben kontrollierten die Forscher in den nächsten Wochen, ob sich die Bakterien im Körper der Tiere hielten und vermehrten.
Das Ergebnis: Die Kontrolltiere zeigten nach drei Wochen klare Anzeichen für eine Tuberkulose-Infektion. Bei den genmanipulierten Kälbern dagegen hatten deutlich weniger Erreger im Körper überlebt. „Die Rinder zeigten eine erhöhte Resistenz gegenüber Mycobacterium bovis“, berichten Zhang und seine Kollegen.
„Damit haben wir eine Technologie und eine günstige Position im Rindererbgut entdeckt, die die Einschleusung nützlicher Gene in diese Nutztiere erlaubt.“ Angesichts der eher geringen Quote erfolgreich geborener Kälber ist allerdings noch einiges an Arbeit nötig, um solche Methoden für die Tierzucht und Landwirtschaft praktikabel zu machen. (Genome Biology, 2017; doi: 10.1186/s13059-016-1144-4)
(BioMed Central, 01.02.2017 – NPO)