Gefährlicher Energiemangel: Forscher haben eine weitere Ursache für den Niedergang von Hirnzellen bei Alzeimer-Patienten entdeckt: die Energieproduktion der Zellkraftwerke bricht bei ihnen zusammen. Dadurch sind die Zellen dem Untergang geweiht. Ursache dafür sind vermutlich Beta-Amyloid-Ablagerungen innerhalb der Hirnzellen, denn sie blockieren den Nachschub der Mitochondrien, wie die Forscher herausfanden.
Im Gehirn von Alzheimer-Kranken finden sich zwischen den Nervenzellen charakteristische Ablagerungen, die sogenannten Plaques. Diese bestehen aus Beta-Amyloiden – das sind kurze Eiweiß-Ketten. Beta-Amyloide kommen auch bei gesunden Menschen vor, werden dort aber schnell abgebaut. Bei Alzheimer-Patienten häufen sie sich dagegen an. Deswegen suchen Forscher laufend nach Verfahren, die die schädlichen Ablagerungen beseitigen und das teilweise schon mit Erfolg.
Liegt der Auslöser im Inneren?
Lange Zeit dachte man, dass die extrazellulären Amyloid-Ablagerungen die Gehirnzellen schädigen und schließlich abtöten. Die großen Mengen miteinander verknäulter Beta-Amyloide wären damit die Triebkraft für das Fortschreiten der Alzheimer-Demenz.
Doch heute weiß man: Auch innerhalb der Nervenzellen kommen Beta-Amyloide vor. Manche Forscher vermuten deswegen, dass sie innerhalb der Zelle ihre toxische Wirkung entfalten, indem sie bestimmte Bestandteile der Zelle schädigen. Giovanna Cenini und ihre Kollegen von der Universität Bonn haben diese Theorie untersucht.
Wirkung auf Mitochondrien getestet
„Wir haben in unserer Arbeit untersucht, ob Beta-Amyloide die Mitochondrien schädigen können“, erklärt Ceninis Kollege Wolfgang Voos. Denn Beobachtungen zeigen, dass diese Kraftwerke der Zelle bei Hirnzellen von Alzheimer-Patienten oft defekt sind. „Dazu haben wir unter anderem isolierte Mitochondrien mit Beta-Amyloiden versetzt und getestet, welche Prozesse dadurch gestört werden“, so Voos weiter.
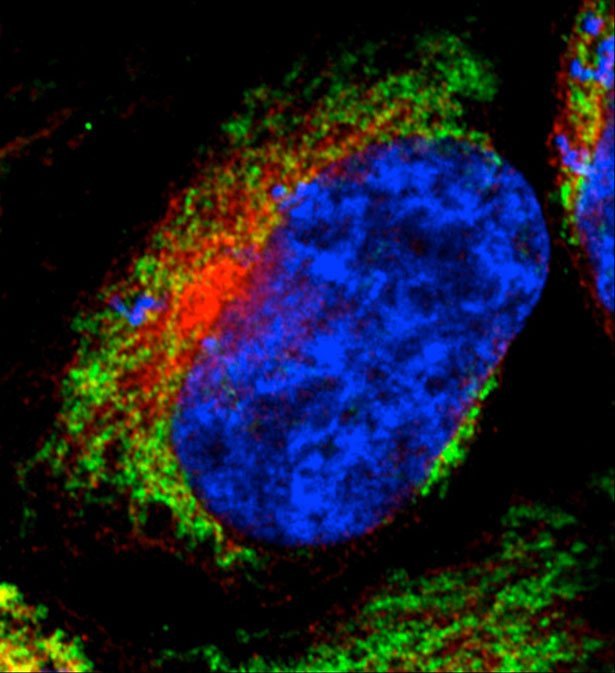
Interessanterweise fanden die Forscher nach der Behandlung aber keine direkten Schäden an den Mitochondrien. Die Zellkraftwerke waren völlig intakt.
Effektive Blockade
Stattdessen entdeckten die Wissenschaftler aber etwas anderes: Die Beta-Amyloide hemmten die Aufnahme von Proteinen. „Ich habe im Laufe meines Forscherlebens selten eine solch starke Blockade des Proteintransports gesehen“, betont Voos. Durch diese Blockade können die Mitochondrien mit der Zeit keine Energie mehr produzieren – und gehen zugrunde.
Für ihre komplexe Aufgabe benötigen die Minikraftwerke rund 1.000 verschiedene Proteine. Gerade einmal 13 davon können sie selbst herstellen. Die restlichen werden im Cytoplasma der Zelle produziert. Die Mitochondrien nehmen sie von dort mit Hilfe spezieller Transporter-Moleküle auf ihrer Oberfläche auf. Diese Aufnahme wird von den Beta-Amyloiden gehemmt – und zwar extrem effektiv, wie die Forscher herausfanden.
Zellen verschleißen
Ähnlich wie eine komplizierte Maschine unterliegen auch Mitochondrien einem ständigen Verschleiß. Viele ihrer Bestandteile haben nur eine begrenzte Lebensdauer und müssen daher regelmäßig ersetzt werden. Ohne den Nachschub verarmen die Zellkraftwerke unter anderem nach und nach an den Enzymen, die sie zur Energieerzeugung brauchen.
„Dieser Mechanismus kann womöglich entscheidend zu dem massenhaften Untergang von Neuronen beitragen, der für die Alzheimer-Demenz charakteristisch ist“, sagt Voos. Allerdings ist noch unklar, ob sich die Ergebnisse aus dem Reagenzglas auf ganze Zellen oder gar Alzheimer-Kranke übertragen lassen, schränken die Forscher ein. „Wir wollen nun in einem nächsten Schritt herausfinden, ob wir die Blockade des Protein-Transports auch in den Nervenzellen von Patienten finden“, so Voos. (Molecular Biology of the Cell, 2016; doi: 10.1091/mbc.E16-05-0313)
(Universität Bonn, 10.10.2016 – HDI)