Eine einzige Aminosäure macht den Unterschied: Ein aus Bananen isoliertes Protein wirkt dank einer winzigen Manipulation effektiv gegen Grippe-, Hepatitis- und AIDS-Viren – ohne die bisherigen Nebenwirkungen. Nun hoffen die Forscher, auf dieser Grundlage Breitband-Medikamente gegen Viren entwickeln zu können, wie sie im Magazin „Cell“ berichten.
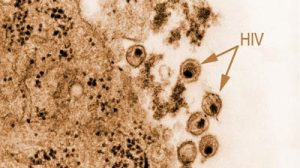
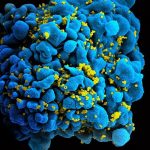
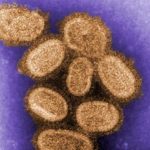
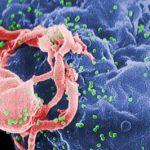
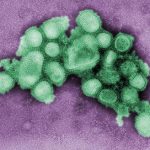
Bananen enthalten ein medizinisch hochinteressantes Protein: Das Bananen-Lektin (BanLec) kann an spezifische Zuckerbausteine auf der Oberfläche von Viren binden. Das bewirkt, dass ein Virus nicht mehr in eine Zelle eindringen kann. Hepatitis C und Grippeviren lassen sich so aufhalten, und selbst das AIDS-verursachende HI-Virus wird von BanLec gestoppt.
Bisher unerwünschte Immunreaktionen
Allerdings hat BanLec auch einen enormen Nachteil: Es wirkt mitogen, das heißt, es regt Zellen zur Teilung an. Da diese Nebenwirkung besonders die T-Zellen des Immunsystems betrifft, kommt es zu unerwünschten Immunreaktionen und Entzündungen. Im Fall von HIV könnte dies noch dazu die antivirale Wirkung ins Gegenteil verkehren, da sich dieses Virus in T-Zellen vermehrt – ihm stünden dann noch mehr Wirtszellen zur Verfügung.
Doch ein Forscherteam um David Markovitz von der University of Michigan hat nun einen Durchbruch erzielt: Sie untersuchten die Struktur des Bananenproteins, um die beiden Wirkungsmechanismen getrennt voneinander beeinflussen zu können. Dann produzierten sie auf molekulargenetischem Wege eine neue Version von BanLec. Sie ersetzten lediglich eine einzige Aminosäure in der Kette des Proteins: An Position 84 tauschten sie Histidin gegen Threonin aus und erhielten so die BanLec-Version H84T.
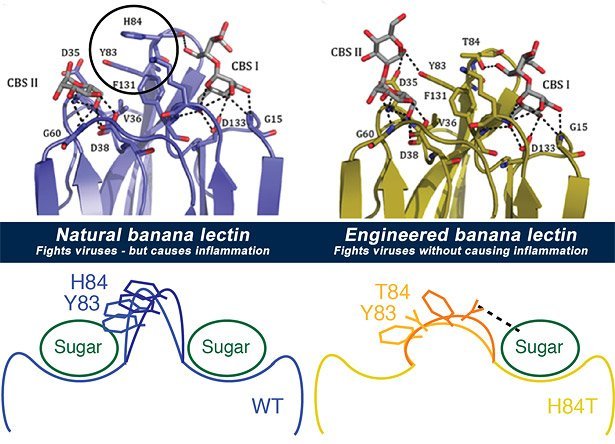
Verändertes BanLec schützt Mäuse vor Grippe
Diese modifizierte Version war in Blut- und Gewebeproben gegen Grippe-, AIDS- und Hepatitis-C-Viren wirksam – und das, ohne die T-Zellen zu stimulieren und so Entzündungen hervorzurufen. In Versuchen an Mäusen zeigten die Forscher außerdem, dass H84T vor der Ansteckung mit Grippe schützt.
„Bessere Grippe-Medikamente sind dringend nötig“, sagt Markovitz und hofft, dass aus BanLec bald schnell einsetzbare Notfallmedikamente hervorgehen. „Was wir hier gemacht haben ist spannend, weil es die Möglichkeit eröffnet, BanLec in ein Breitband-Mittel gegen Viren weiterzuentwickeln“, sagt Studienleiter Markovitz. Damit ließen sich beispielsweise Epidemien bereits bekämpfen, noch bevor der genaue Erreger bekannt ist.
Gesamtbild aus einzelnen Puzzleteilen
Zuckerstrukturen wie die von BanLec anvisierten Mannose-Reste kommen auf vielen Viren vor, die Interaktionen zwischen diesen Zuckern und den Lektinen sind bislang aber nur wenig erforscht. Daher markiert H84T auch einen großen Erfolg in diesem Bereich: „Mit der neuen Studie haben wir es erstmals geschafft, einzelne Puzzleteile der Lektin-Zucker-Interaktion zu einem Gesamtbild zusammenzulegen“, erklärt Koautor Gabius von der Ludwig-Maximilians-Universität München. „Dies ist nicht nur für die Wirkstoffforschung ein großer Fortschritt, sondern kann auch unser Verständnis des Zucker-Codes einen wichtigen Schritt weiterbringen.“
Das modifizierte BanLec soll nun auf breiter Basis gegen verschiedene Viren getestet werden. Außerdem wollen die Wissenschaftler auch körpereigene Lektine im Hinblick darauf testen, ob sie für verschiedene Anwendungsmöglichkeiten optimiert werden können. „Ein Vorteil solcher maßgeschneiderten Lektine wäre auch, dass die Wahrscheinlichkeit von Resistenzen geringer ist, da Zuckerstrukturen konstanter sind als die Proteinstrukturen von Antikörpern“, sagt Gabius. ()
(Ludwig-Maximilians-Universität München / University of Michigan Health System, 23.10.2015 – AKR)