Fußbälle, Ketten und Raupen – bestimmte Makromoleküle bilden Nanopartikel, die sich wiederum selbstständig zu vorbestimmten Strukturen zusammenfügen. Ein deutsches Wissenschaftlerteam hat nun im Magazin „Nature“ einen Prozess beschrieben, in dem sich solche Strukturen gezielt bilden und untersuchen lassen. Durch zahlreiche Kombinationsmöglichkeiten sollen die Winzlinge neue Technologien ermöglichen.
Löst sich Seife in Wasser auf, so sammeln sich die Seifenmoleküle in kugelförmigen Tröpfchen, so genannten Mizellen. Sie entstehen aufgrund der unterschiedlichen Löslichkeit der Molekülenden: Das eine Ende ist wasserlöslich und weist nach außen in Richtung Wasser. Das andere Ende ist fettlöslich und somit wasserabweisend. Diese Enden der Moleküle ballen sich im inneren der Mizelle zusammen. Solche Mizellen sind eins der einfachsten Beispiele, wie sich Moleküle von selbst zu übergeordneten Strukturen zusammenfinden. Diesen Prozess bezeichnet man als Selbst-Aggregation.
Die Nanotechnologie versucht dieses aufbauende Prinzip von kleinen Bausteinen zu zusammenhängenden Strukturen zu kopieren, indem sie die Fähigkeit von Nanopartikeln zur selbständigen Strukturbildung nutzt. Die Erkenntnisse eines Teams von Forschern verschiedener deutscher Universitäten sollen nun helfen, diese Prozesse besser zu verstehen. Die Wissenschaftler untersuchten, wie sich die Struktur einzelner Bausteine auf die bei der Selbst-Aggregation entstehende Form auswirkt.
Von Makromolekülen zu Nanopartikeln
Ausgangspunkt für das nun veröffentlichte Prinzip der Selbst-Aggregation sind so genannte Triblock-Terpolymere, kettenartige Makromoleküle mit einer Größe zwischen 10 und 20 Nanometern. Diese Bausteine bestehen aus jeweils drei linearen „Blöcken“, die kettenartig miteinander verbunden sind. Die Forschungsgruppe konnte solche dreiteiligen Makromoleküle nun dazu veranlassen, sich zu Nanopartikeln mit einem Durchmesser von rund 50 Nanometern zusammenzuschließen.
Die Wissenschaftler verwendeten dabei zwei verschiedene Sorten von „Triblock-Terpolymeren“. Diese unterscheiden sich einzig im mittleren der drei einzelnen Blöcke: Die einen Makromoleküle haben die Struktur „A – B – C“, die anderen die Struktur „A – D – C“. Erstere verknüpfen sich nur an einer Stelle mit anderen Makromolekülen. Dadurch finden sie sich zu kugelartigen Überstrukturen zusammen, die an Fußbälle erinnern. Die andere Abfolge von Blöcken sorgt für zwei Bindungsstellen, wodurch sich die Bausteine in ketten- oder wurmartigen Überstrukturen organisieren.
Entscheidend ist dabei: In beiden Fällen ist die Struktur der entstehenden Nanopartikel durch die zugrunde liegenden Makromoleküle vorprogrammiert, ähnlich wie die Struktur eines Proteins durch die Abfolge der Aminosäuren vorherbestimmt wird. Die Art des einzelnen Bausteins bestimmt die Art der Gesamtstruktur.
Die Mischung macht’s: Von Nanopartikeln zu „Raupenmizellen“

Mit den Fußbällen und Würmern ist der Prozess der Selbst-Aggregation aber noch nicht beendet.
In einem weiteren Schritt mischten die Polymerchemiker die beiden unterschiedlich strukturierten Bausteine so, dass sie gemeinsam eine völlig neue Überstruktur bilden. Darin wechseln sich Fußball- und Wurm-Elemente in genau definierter Weise ab. Diese gemeinschaftliche Anordnung verschiedener Bausteine bezeichnen die Wissenschaftler als Co-Aggregation.
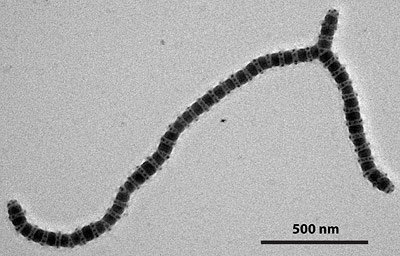
Die neu-entstehende übergeordnete Struktur hat unter dem Elektronenmikroskop starke Ähnlichkeit mit einer Schmetterlingsraupe. Diese besteht gleichfalls aus klar voneinander abgegrenzten, regelmäßig aufeinander folgenden Abschnitten. Die Forschungsgruppe hat deshalb für diese durch Co-Aggregation gebildete Großstruktur den Begriff „Raupenmizelle“ geprägt.
Kombinationsmöglichkeiten sind endlos
Die Raupenmizellen sind keineswegs die einzigen Großstrukturen, die sich aus den durch Selbst-Aggregation gebildeten Nanopartikeln herstellen lassen. „Diese Nanopartikel können zum Beispiel auch mit anorganischen oder biologischen Nano- und Mikropartikeln kombiniert werden, sodass bisher unbekannte Funktionsmaterialien entstehen. Die Kombinationsmöglichkeiten sind schier endlos“, so Müller.
Besonders attraktiv ist dabei die Vielzahl an Makromolekülen, die als Grundbaustein in Frage kommen. Sie können dazu dienen, bestimmte Funktionalitäten gezielt in die angestrebten Großstrukturen einzuschleusen. Solche Strukturen könnten licht- oder temperaturempfindlich sein, oder auch auf elektrische oder magnetische Felder reagieren. Mit solchen schaltbaren Nanopartikeln ist es zum Beispiel denkbar, Medikamente gezielt zu bestimmten Zeiten und an bestimmten Stellen im Körper freizusetzen.
Makromoleküle, die der Polymerforschung als Träger bestimmter Funktionalitäten zur Verfügung stehen, können hundertmal kleiner als ein Mikrometer sein. Dementsprechend hoch ist die Feinheit von übergeordneten Strukturen, die letztlich aus ihnen hervorgehen. „Zukünftige Technologien – wie etwa maßgeschneiderte künstliche Zellen, Transistoren oder Elemente für die Mikro-/Nano-Robotik – können von dieser geringen Auflösungsgrenze erheblich profitieren“, erklärt Müller.
(Nature, 2013; doi: 10.1038/nature12610)
(Universität Bayreuth, 04.11.2013 – AKR)