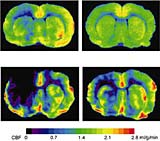
Wissenschaftler haben eine neue Methode zur Schlaganfall-Vorbeugung entwickelt. Im Tierversuch stimulierten sie im Gehirn die Bildung von neuen Blutgefäßen, die einen effizienten Ersatzkreislauf aufbauten. Im Idealfall kann die Durchblutungsstörung so voll kompensiert und ein Hirninfarkt verhindert werden.
Todesursache Schlaganfall
Der Schlaganfall ist nach Herzinfarkt und Krebs die dritthäufigste Todesursache in Deutschland – 20 Prozent der über 65-Jährigen sind davon betroffen, in zehn Prozent der Fälle endet er tödlich. Auslöser ist ein plötzlicher Gefäßverschluss (ischämischer Schlaganfall) oder eine Blutung im Bereich des Gehirns. Für die Behandlung des Schlaganfalls gibt es trotz beachtlicher Fortschritte im Verständnis der molekularen Schädigungsmechanismen nach wie vor keine klinisch gesicherte medikamentöse Therapie. Wissenschaftler suchen daher schon seit längerem nach Möglichkeiten für eine wirkungsvolle Vorbeugung, bei Risikopatienten.
Ein neues Verfahren, das hierfür geeignet scheint, ist durch Medikamente ausgelöste Stimulation der Arteriogenese, der Ausbildung von Kollateral- oder Umgehungsgefäßen im Gehirn. Diese spielen bei Gefäßverschlüssen eine bedeutende Rolle für die Wiederherstellung der Durchblutung. Ausgelöst wird ihre Bildung durch mechanische Laständerungen an den zuführenden Adern; nach Verschluss eines Blutgefäßes erhöhen sich infolge der Umverteilung der Stromrichtung die mechanischen Scherkräfte des Blutes. Da der Strömungswiderstand mit dem Gefäßdurchmesser abnimmt, das Blut durch die sehr dünnen Kollateralgefäße also viel schneller strömt als durch die großen Gefäße, wird durch das Kollateralwachstum ein effizienter Ersatzkreislauf aufgebaut, der im Idealfall die Durchblutungsstörung voll kompensiert.
Für den Herzkreislauf und die peripheren Durchblutungsstörungen konnten Wissenschaftler vom Max-Planck-Institut für physiologische und klinische Forschung in Bad Nauheim dieses bereits mit Erfolg zeigen, insbesondere wenn die Arteriogenese pharmakologisch durch biologische Faktoren wie den Granulozyten-Makrophagen Kolonie-stimulierender Faktor (GM-CSF) angeregt wird.
Blutgefäßbildung auch im Gehirn auslösbar
Am Max-Planck-Institut für neurologische Forschung in Köln wurde jetzt in Zusammenarbeit mit der Forschergruppe für experimentelle und klinische Arteriogenese der Universität Freiburg erstmals gezeigt, dass auch im Gehirn die Arteriogenese von Kollateralgefäßen ausgelöst und damit eine wirkungsvolle Vorbeugung für den Schlaganfall erreicht werden kann.
Um einen künstlichen Schlaganfall auslösen zu können, wurden bei den Versuchstieren die beiden Vertebralarterien und eine der beiden Halsschlagadern verschlossen. Das Gehirn wird dadurch nur noch von einer einzigen Halsschlagader versorgt; ein Kollateralsystem an der Hirnbasis, das Circulus Willisii, hält den Blutzustrom zu den ursprünglich von den anderen drei Gefäßen versorgten Hirngebieten aufrecht. Die Hirndurchblutung sinkt nach diesem Eingriff auf etwa 50 Prozent des Ausgangswertes ab, was zwar noch keine Hirnschädigung, wohl aber ein stark erhöhtes Risiko für den Eintritt eines Schlaganfalls bewirkt.
Wird jetzt der Blutdruck gesenkt, ist die Kollateralversorgung nicht mehr in der Lage, eine ausreichende Durchblutung aufrecht zu halten, und es kommt auf der Seite, auf der die Halsschlagader verschlossen wurde, innerhalb weniger Minuten zur Ausbildung eines Hirninfarktes. Dieses Risiko wird durch Auslösen der Arteriogenese im Circulus Willisii deutlich reduziert. Wie die Kölner Neurologen zeigen konnten, kommt es spontan zu einer Verbesserung der Blutzufuhr in die gefährdete Hirnhälfte, welche bei den pharmakologisch mit GM-CSF behandelten Tieren aber deutlich verstärkt und beschleunigt ist.
Kohlensäure-Gehaltes des Blutes untersucht
Als Referenzwert erfassten die Wissenschaftler die Erhöhung des Kohlensäure-Gehaltes des Blutes. Er ist ein Maß für die so genannte hämodynamische Reservekapazität und gibt an, über welche Kompensationsmechanismen das beeinträchtigte Hirngefäßsystem noch verfügt. Bereits eine Woche nach Therapiebeginn, d.h. Injektion von GM-CFS, vergrößerte sich der Gefäßdurchmesser im Circulus Willisii bei den Versuchstieren um mehr als 100 Prozent, die Durchblutung des Gehirns und die hämodynamische Reservekapazität normalisierten sich, und der durch eine Blutdrucksenkung ausgelöste Hirninfarkt verkleinerte sich um mehr als die Hälfte.
„Für den klinischen Schlaganfall eröffnen diese Befunde interessante Perspektiven“ erklärt Konstantin-Alexander Hossmann. „Die Messung der so genannten hämodynamischen Reservekapazität ist eine klinisch etablierte Methode, um Risikopatienten frühzeitig vor Eintritt eines Schlaganfalls identifizieren zu können. Sollte sich herausstellen, dass bei diesen Patienten ebenso wie in unseren Tierversuchen eine Arteriogenese induziert und die hämodynamische Reserve wiederhergestellt werden kann, wäre dies eine sehr effiziente Methode, um den Eintritt eines Schlaganfalls zu verhindern.“ Der Max-Planck-Forscher plädiert daher für baldige klinische Untersuchungen, um diese neue Therapie zu erproben.
Die Forscher berichten in der neuesten Ausgabe der Proceedings of the National Academy of Science über ihre Ergebnisse.
(idw – MPG, 21.09.2004 – DLO)