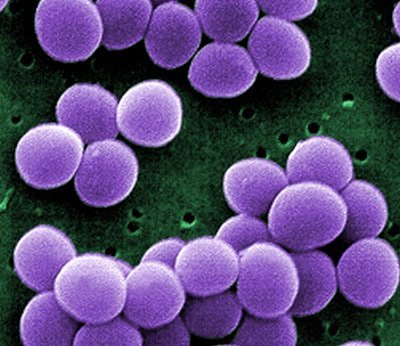
Eine neue Strategie könnte gegen die Ausbreitung von Antibiotika-Resistenzen helfen: Man hindert die resistenten Bakterien einfach am Sex und damit am Genaustausch. Wie das funktionieren kann, haben US-amerikanische Forscher jetzt am gefährlichen Krankenhauskeim Staphylococcus aureus herausgefunden. Demnach reicht die Blockade einer Andockstelle an einem Enzym des Bakteriums aus, wie sie im Fachmagazin „Proceedings of the National Academy of Sciences“ berichten.
Allein in Europa infizieren sich jährlich mehrere hunderttausend Menschen mit einem resistenten Erreger, einige zehntausend sterben daran. Denn diese krankmachenden Bakterien sind gegen eines oder sogar mehrere der gängigen Antibiotika immun – die einst wirksamste Waffe der Medizin ist gegen sie machtlos. Einer der verbreitetsten multiresistenten Erreger ist das Bakterium Staphylococcus aureus (MRSA). Anfangs nur gegen Penicillin und Substanzen der gleichen Wirkstoffklasse immun, verbreiten sich seit einigen Jahren in Krankenhäusern weltweit auch MRSA-Stämme, die zusätzlich gegen das Reserveantibiotikum Vancomycin resistent sind. Erhalten haben sie diese Resistenz durch Gentransfer von einem anderen Bakterium.
Enzym im Visier
Jonathan Edwards von der University of North Carolina in Chapel Hill und seine Kollegen haben nun genauer untersucht, welcher Mechanismus die MRSA-Keime dazu befähigt, sich mit einem anderen Keim zusammenzulagern und DNA auszutauschen. Denn die genaue Kenntnis dieses Prozesses könnte, so ihre Hoffnung, Ansatzpunkte liefern, um genau diesen Mechanismus des Resistenzerwerbs zu blockieren und so zu verhindern, dass sich die Resistenzen noch weiter ausbreiten als ohnehin schon.
Für ihre Studie nahmen sie dafür ein spezielles Enzym genauer unter die Lupe, das sogenannte Nicking-Enzym. „Dieses Enzym initiiert und terminiert den Transfer von Plasmiden, wenn sich zwei Bakterien zusammenlagern“, erklären sie. Plasmide sind kleine DNA-Ringe, die bei Bakterien lose im Zellinneren liegen und daher leicht von einer Zelle zur anderen ausgetauscht werden können. Auf ihnen liegen häufig die Gene, die die Keime unempfindlich gegen bestimmte Wirkstoffe machen.
Andockstelle blockiert
Mit Hilfe von röntgenkristallografischen Aufnahmen analysierten die Wissenschaftler erstmals die genaue Struktur und Funktionsweise des MRSA- Nicking-Enzyms. Ihre Analysen ermöglichten es ihnen, zu rekonstruieren, wie sich die verschiedenen Komponenten des Enzyms an die DNA eines Plasmids anlagern und dieses für den Transfer vorbereiten. Dabei zeigte sich, dass zwei Andockstellen dieses Proteinkomplexes für diese Bindung unverzichtbar sind. „Das Wissen um diese strukturellen Details eröffnet uns neue Strategien, um den Erwerb neuer Resistenzen bei Erregern zu verhindern“, betonen Edwards und seine Kollegen.
Wie diese Strategien konkret aussehen könnten, testeten die Forscher in einem nächsten Schritt. Sie entwickelten ein synthetisches Polymer, das die Bindung einer der Andockstellen des Nicking-Enzyms an die Plasmid-DNA blockiert. Dazu lagert es sich an einem bestimmten Strukturteil der DNA an und versperrt dem Enzym damit den Zugang. Gaben die Wissenschaftler diese Substanz zu einer Lösung mit Nicking-Enzym und Plasmiden, reichte schon eine geringe Menge des Polymers aus, um die Enzymfunktion zu hemmen. Mit diesem und ähnlichen Hemmstoffen könnte sich daher zukünftig eine neue Möglichkeit eröffnen, die Ausbreitung von Resistenzen bei MRSA zu verhindern, so das Fazit der Forscher. (Proceedings of the National Academy of Sciences (PNAS), 2013; doi: 10.1073/pnas.1219701110)
(Proceedings of the National Academy of Sciences, 29.01.2013 – NPO)