Zum ersten Mal ist es Forschern gelungen, die molekulare Ansatzstelle einer Antibiotika-Resistenz aufzuklären, bevor resistente Krankheitserreger die klinische Anwendung des Wirkstoffs wirkungslos machen. Wie sie in der Fachzeitschrift „FEBS Letters“ berichten, vermittelt die Struktur des Proteins Monooxygenase TetX den Bakterien eine Resistenz gegen neue Tetracyclin-Antibiotika. Damit ist nun ein schpützender Umbau des gefährdeten Antibiotikas Tigecyclin möglich.
Die Entwicklung und Anwendung von Antibiotika zur Behandlung von bakteriellen Infektionskrankheiten wird seit langer Zeit durch die Ausbreitung klinisch problematischer Resistenzmechanismen immer schwieriger und kostspieliger. Wird ein neuer Wirkstoff nach jahrelanger Entwicklung auf den Markt gebracht, dauert es nicht lange, bis resistente Mikroorganismen bekannt werden – ein ewiges Wettrüsten.
Resistenz auch schon auf neue Tetracyclin-Variante
Kürzlich wurde die Tetracyclin-Variante Tigecyclin in die klinische Anwendung aufgenommen. Von diesem Antibiotikum ist bekannt, dass es gegen resistente Bakterien hochwirksam ist. Leider ist auch hier bereits ein bakterieller Resistenzmechanismus bekannt, der momentan zwar noch keine Rolle bei der Anwendung in der Human- und Tiermedizin spielt. Aber es steht zu befürchten, dass sich dieser
Mechanismus auf problematische Krankheitskeime ausbreiten wird.
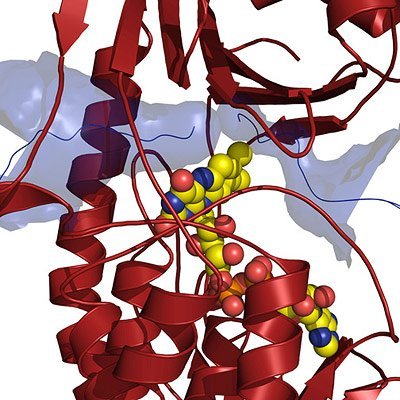
In enger Kooperation mit Wissenschaftlern der McMaster Universität in Kanada und des Helmholtz-Zentrum Berlin für Materialien und Energie haben Forscher um Professor Winfried Hinrichs im Institut für Biochemie der Universität Greifswald mit Methoden der Proteinkristallographie die dreidimensionale Struktur des Resistenzproteins aufgeklärt. Sie stellten fest, dass die Resistenz auf einem Enzym beruht, der Monooxygenase TetX. Es versetzt die Bakterien in die Lage, alle medizinisch relevanten Tetracycline gezielt abzubauen.
Struktur der Resistenz-Ansatzstelle entschlüsselt
Röntgen-kristallographischen Untersuchungen, durchgeführt an Synchrotron- Strahlungsquellen in Hamburg (EMBL c/o DESY) und Berlin (BESSY geben Einblick in die atomare Struktur des Enzym-Moleküls und zeigen, wie Tetracycline erkannt werden. Damit ist der einzigartige Fall eingetreten, dass ein Schlüsselschritt eines Resistenzmechanismus auf molekularer Ebene bekannt ist, noch bevor das Antibiotikum wirkungslos wird. Auf dieser Basis könnte es möglich werden, Konzepte zu entwickeln, wie neue Tetracyclin-Moleküle umzubauen sind, damit sie gegen TetX stabil sind und wieder antibiotische Wirkung haben („drug design“). (FEBS Letters 585(7), 1061-1066 (2011))
(Universität Greifswald, 26.04.2011 – NPO)