Ein Forschertraum seit mehr als einem Jahrzehnt ist nun wahr geworden: Erstmals ist es einem internationalen Forscherteam gelungen, biologische Strukturen ohne vorherige langwierige Kristallisation hochauflösend abzubilden. Dies gelang mit Hilfe eines starken Röntgenlasers, der Aufnahmen durch ultrakurze und extrem intensive Röntgenblitze machte. Die Experimente, in gleich zwei Beiträgen in der aktuellen „Nature“ veröffentlicht, sind ein erster und entscheidender Schritt, um molekulare Strukturen von Proteinen oder Viren ohne aufwändige Kristallisation bestimmen zu können.
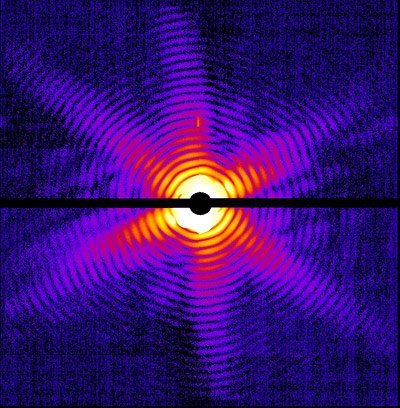
Die 3D-Strukturen von Proteinen und Viren werden üblicherweise mit Hilfe der so genannten Röntgenkristallographie aufgezeichnet. Dabei trifft ein Röntgenstrahl auf den Kristall, und es entsteht eine Anordnung von Punkten, das so genannte Röntgenbeugungsmuster. Während der Kristall im Röntgenstrahl gedreht wird, gibt die gemessene Intensität dieser Punkte ein dreidimensionales Abbild der Probe. Allerdings werden die Testobjekte bei der Untersuchung von der intensiven ionisierenden Strahlung zerstört. Deshalb sind große und aufwändig herzustellende Kristalle notwendig, um deutliche Beugungsmuster zu erzielen, bevor die Zerstörung einsetzt. Dieses Verfahren scheitert daher oft daran, dass eine einwandfreie Kristallisation von vielen Biomolekülen nicht möglich ist.
Ultrakurze Röntgenblitze ermöglichen Schnappschüsse ohne große Kristalle
Neu entwickelten Freie-Elektronen-Laser produzieren jedoch so ultrakurze, extremhelle Lichtblitze, dass sich mit ihnen Bilder aufnehmen lassen, bevor der Zerstörungseffekt eintritt. Der Freie-Elektronen-Laser LCLS in Stanford produziert Röntgenblitze, die so intensiv sind, dass jede Probe in dem Strahl zu einem Plasma verdampft. Doch der Blitz erzeugt kurz vorher, in nur 100 Femtosekunden, die Aufnahme. Die Blitze sind zudem so intensiv, dass die Beugungsmuster winziger Nanokristalle oder sogar einzelner Viruspartikel intensiv genug für die Auswertung sind – ohne dass erst mühsam große Kristalle gezüchtet werden müssen.
Experiment belegt Funktionieren des Prinzips
Das dieses theoretisch schon seit längerem bekannte Prinzip auch wirklich bei den kleinsten Biomolekülen funktioniert, hat jetzt ein internationales Forscherteam unter Leitung von Professor Henry Chapman vom Center for Free-Electron Laser Science (CFEL) bei DESY in Hamburg am Freie-Elektronen-Laser LCLS an Proteinen und Viren nachgewiesen. „Diese Experimente sind ein Durchbruch auf unserem Weg zur Röntgenbeugung von Einzelobjekten“, so Professor Helmut Dosch, Vorsitzender des DESY- Direktoriums. „Wir schauen in die Welt von morgen, in der wir Aufnahmen von nicht-kristallinem Material mit Röntgenlasern in den Griff bekommen werden.“

1.800 Beugungsmuster pro Minute
Die in Nature veröffentlichten Studien präsentieren das Konzept „diffraction before destruction“ in spektakulärer Weise. Jeder Röntgenblitz ergibt ein einzelnes Bild von dem Objekt. Zur Erzeugung einer 3D-Abbildung werden viele Schnappschüsse von zufällig ausgerichteten, identischen Objekten genutzt. Die Zielobjekte werden in einem Aerosolstrahl oder in einem gasfokussierten Flüssigkeitsstrahl dem Röntgenstrahl ausgesetzt. Mit diesem Versuchsaufbau erzeugten die Wissenschaftler 1.800 einzelne Beugungsmuster pro Minute. Vor jedem Röntgenblitz – 30 pro Sekunde – wurde ein neues Teilchen eingefügt, um das vorher verdampfte zu ersetzen.
Die Hochgeschwindigkeits-Röntgendetektoren erfassten und digitalisierten mehrere Tage lang Millionen von Beugungsmustern. Das ergab mehrere Terabyte an Daten – die Datenrate lag höher als die der Teilchenphysikexperimente am Large Hadron Collider (LHC). Die Daten wurden an Computer-Clustern bei DESY und SLAC analysiert. Hierzu wurden mit parallelen Programmen die 3D Beugungsmuster bestimmt, die aus Zehntausenden der besten Beugungsmuster zusammengesetzt sind. Dieses Muster entsprach dann dem eines einzelnen perfekten Kristalls.
Photosystem-I aus Minikristallen abgebildet
In ihren Experimenten machten die Forscher Aufnahmen von dem so genannten Photosystem-I-Protein-Komplex und dem Mimivirus. Photosystem-I ist eine entscheidende Komponente zur Umwandlung des Sonnenlichts in Energie mittels Photosynthese. Die Kristalle mit einer Größe von nur 100 Nanometern bis zwei Mikrometern wurden von Professor Petra Fromme von der Arizona State University produziert. Sie gehören zu den membrangebundenen Proteinen, die extrem empfindlich und schwer in kristalline Form zu bringen sind.
Die Struktur des Photosystem-I-Komplexes wurde zwar vor kurzem ermittelt, aber nur mit Hilfe von großen Kristallen. Man benötigte dafür allein 13 Jahre, um die Kristallisationsbedingungen zu erkennen. Dies ermöglichte jetzt einen quantitativen Vergleich, der die Genauigkeit der FEL-Methode unter Nutzung der wesentlich einfacher herzustellenden Nanokristalle unter Beweis stellte. Es zeigte sich, dass ein Beugungsbild vor der Zerstörung mit solch extrem empfindlichen Objekten realisierbar ist.
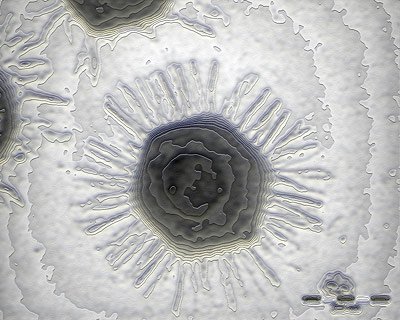
Erster Schnappschuss eines Virus ohne Kristallisation
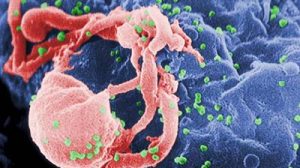
In einem weiteren Experiment gelang den Wissenschaftlern der Nachweis, dass Kristallisation sogar komplett vermieden werden kann. Mit einem noch genauer fokussierten Blitz bildeten sie einzelne Exemplare des Mimivirus ab, des größten bekannten Virus, der Amöben befällt. Tausende Beugungsmuster von einzelnen Viren wurden aufgezeichnet und ihre einzelnen Bilder rekonstruiert. Diese neue Art der Bildgebung macht ein Einfrieren, Zerschneiden oder chemische Markierung der Struktur überflüssig, sie könnte sich sogar für ganze lebende Zellen eignen. Um auch die Beugungsmuster von einzelnen Molekülen aufzeichnen zu können, ohne dass eine Kristallisation notwendig ist, bedarf es noch weiterer Entwicklungen. Dabei müssen die Röntgenblitze auf noch kleinere Punkte fokussiert werden, um ihre Intensität zu vergrößern.
Möglich nur dank internationaler Kooperation
„Diese Ergebnisse sind der Höhepunkt langjähriger Arbeit, die hier bei DESY mit Experimenten an FLASH, dem Freie-Elektronen Laser in Hamburg, ihren Anfang nahmen“, so Chapman. „Obwohl unsere aus einzelnen Nanokristallen erzielten Röntgenstrukturen exakt den in den Lehrbüchern gemachten Voraussagen entsprachen, waren wir überrascht und begeistert, wie gut die Experimente funktionierten. Dies war nur möglich mit einem interdisziplinären Forscherteam aus Physikern, Biologen und Experten im Bereich Optik, Plasmen und Detektoren.“
Die Arbeitsgruppe, die dieses Pionier-Experiment durchgeführt hat, besteht aus 85 Mitgliedern von CFEL bei DESY, Arizona State University, Max- Planck-Institut für Medizinische Forschung und der Max Planck Advanced Study Group am CFEL, Universität Uppsala, SLAC, Stanford PULSE Institute, Lawrence
Livermore National Laboratory und Lawrence Berkeley National Laboratory. Die von dieser Gruppe dargestellten Verfahren werden noch weiter entwickelt, um eine höhere Auflösung zu erzielen. Diese Forschung zeigt bereits jetzt das enorme Potenzial von Freie- Elektronen-Röntgenlasern, wie zum Beispiel auch dem European XFEL in Hamburg. (Nature, 2011; doi:10.1038/nature09750 und doi:10.1038/nature09748)
(Deutsches Elektronen-Synchrotron DESY, 03.02.2011 – NPO)