Drehen, schütteln und beiseite rücken – eine ausgeklügelte Choreografie sorgt in lebenden Zellen dafür, dass Aminosäuren in der vorgesehenen Reihenfolge verknüpft werden, wenn Proteine synthetisiert werden. Forscher haben jetzt mit bisher ungekannter Genauigkeit nachgezeichnet, welche komplizierten Bewegungen dabei ablaufen und berichten über ihre Erkenntnisse in der aktuellen Ausgabe der Wissenschaftszeitschrift „Nature“.
Eiweiße entstehen im Zusammenspiel zweier Ribonukleinsäuren (RNA) in den Ribosomen, den „Eiweißfabriken“ der Zelle. Dabei wird der Bauplan der Eiweiße, die so genannte Boten-RNA, wie ein Magnetfilm an der Nahtstelle zwischen den beiden Untereinheiten des Ribosoms abgelesen. Anschließend werden die Eiweiße kettenartig aus Aminosäuren aufgebaut.
Von der Nukleinsäurewelt zur Proteinwelt
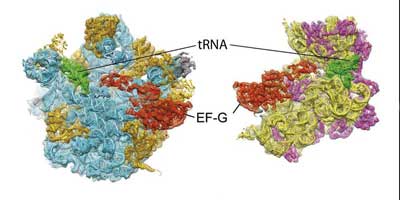
Leser der Boten-RNA und gleichzeitig Träger der Aminosäuren sind die Transfer-RNA (tRNA). Diese transportieren die zum Aufbau der Eiweiße benötigten Aminosäuren solange zum Ort der Synthese, bis der Bauplan das Ende dieser Arbeit signalisiert.
Damit ist der genetische Code, der in der Abfolge der Nukleinsäuren gespeichert ist, von der Nukleinsäurewelt in ein Produkt der Proteinwelt übersetzt worden. Das fertige Eiweiß verlässt dann über einen Tunnel das Ribosom. Unklar war bislang, wie die Boten-RNA und die Transfer-RNA durch das Ribosom bewegt werden.
Ortswechsel der tRNA-Moleküle im Visier
Die beteiligten Wissenschaftler aus Berlin, Marburg, München, Frankfurt/Main, Los Alamos, San Diego, Tallahassee und Houston sind nun der Frage nachgegangen, wie der Ortswechsel der tRNA-Moleküle im Detail vor sich geht – ein anspruchsvolles Unterfangen, weil die Bewegung sehr schnell vor sich geht, so dass sie nur schwer zu beobachten ist.
Die internationale Arbeitsgruppe rekonstruierte deshalb die aufeinander folgenden Zustände des Ribosoms, indem ein Team um Professor Christian Spahn an der Charité in Berlin die Methode der dreidimensionalen Kryo-Elektronenmikroskopie nutzte. „Bei diesem Verfahren werden die Ribosomen in flüssigem Ethan bei – 192° Celsius schockgefroren und mehrere 100.000 zweidimensionale Einzelbilder in zwei dreidimensionale Rekonstruktionen zurückprojiziert“, erläutern die Wissenschaftler in Nature.
tRNA mit drei Positionen
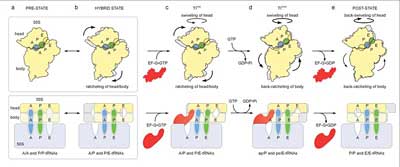
Für die tRNA lassen sich den Forschern zufolge drei Positionen unterscheiden: An der ersten bindet die tRNA ans Ribosom, wobei sie eine Aminosäure trägt (A-Position). An der zweiten hat sie die Aminosäure abgegeben (P) und an der dritten verlässt die tRNA das Ribosom (E). Den Forschern ist es nun gelungen, einen neuartigen Übergangszustand zu identifizieren, bei dem sich die tRNA zwischen zwei dieser Positionen befindet.
Wie die Wissenschaftler darüber hinaus feststellten, geht dieser Transport mit festgelegten Bewegungen des Ribosoms einher: Dessen beide Untereinheiten vollführen gegenläufige Drehungen und schieben dadurch die tRNA von einer Position zur nächsten. Hierbei gewährleistet das EF-G-Enzym, dass die Bewegungsrichtung beibehalten wird – wie ein Türstopper, der das Zurückschwingen verhindert.
tRNA-Transport durch Drehung, Einrasten und Entsperren des Ribosoms erleichtert
„Unsere Einblicke in die Struktur der tRNA-Zustände legen ein Modell nahe, bei dem der tRNA-Transport durch Drehung, Einrasten und Entsperren des Ribosoms erleichtert werden“, fassen die Forscher ihre Ergebnisse zusammen. „Diese Befunde erlauben unmittelbare strukturelle und mechanistische Einsicht in die Zwischenprodukte, die an der universell konservierten Translokation beteiligt sind.“
(Universität Marburg / Charité-Universitätsmedizin Berlin, 03.12.2010 – DLO)