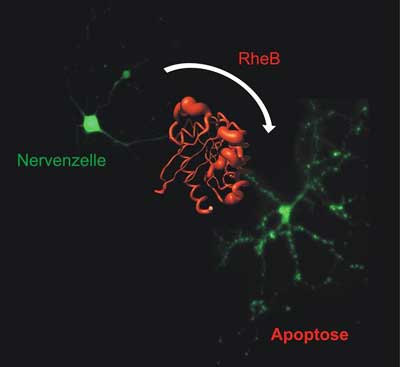
Das Signalprotein Rheb kommt in vielen Körperzellen, besonders im Gehirn vor. Es ist wichtig für Wachstumsprozesse – bei Zellstress zeigt es aber sein zweites Gesicht. In diesem Fall beschleunigt es den Tod der Zelle. Dies haben jetzt Bochumer Forscher in einer neuen Studie heraus gefunden.
Die Ergebnisse haben Auswirkungen auf die Behandlung von Erkrankungen: Das verbreitet eingesetzte Antibiotikum Rapamycin, das die Signalweiterleitung von Rheb verhindert, sollte mit Bedacht eingesetzt werden, raten die Forscher um Professor Rolf Heumann und Professor Raphael Stoll von der Ruhr-Universität Bochum im „Journal of Biological Chemistry“. Unter Zellstressbedingungen könnte sich seine Wirkung umkehren.
Ein Protein, viele Funktionen
Um seine Wirkung entfalten zu können, muss der Signalweg von Rheb – Ras homologue enriched in brain – aktiviert werden. Das geschieht den Forschern zufolge unter anderem durch die Bindung von aktiviertem Rheb an die Protein-Kinase mTOR (target of rapamycin). Der gebundene Komplex verursacht über weitere Signalkaskaden Zellwachstum, Steuerung des zellschützenden kontrollierten Abbaus von Zellbestandteilen – Autophagie -, der Reaktionen der Zelle auf Energieverknappung und der Proteinherstellung.
Das Antibiotikum Rapamycin hemmt die mTOR-Kinase und somit auch die Aktivierung durch Rheb. Es wird bereits vielfach in der medizinischen Praxis angewendet, beispielsweise als Mittel zur Unterdrückung der Immunantwort oder bei der Krebstherapie zur Verhinderung von Zellwucherung.
Ähnlichkeit mit Ras
Rheb hat große Ähnlichkeit mit dem Produkt des Krebsgens Ras. Ras ist Mitglied einer Proteinfamilie, die weitreichende Signalsysteme für nahezu sämtliche zellulären Prozesse steuert.
„Wir wollten wissen, ob die Funktion und Struktur des Rheb denen von Ras ähnlich sind“, erläutert Heumann. „Da wir schon früher zeigen konnten, dass Ras Nervenzellen nach Verletzungen vor dem Zelltod schützt, die Zahl der Verschaltungen zwischen Nervenzellen im Gehirn erhöht und das Volumen der Nervenzellen vergrößert, haben wir nachgeforscht, ob Rheb ebenfalls diese Wirkungen hat.“
Flexible Schalter
Zu ihrer großen Überraschung fanden die Forscher jedoch heraus, dass Rheb nach bestimmten Stress-Behandlungen wie UV-Bestrahlung die Zelle nicht vor dem Zelltod schützt, sondern ganz im Gegenteil ihren Untergang – die Apoptose – noch verstärkt. Um den Ursachen dieses gravierenden Unterschieds zu Ras auf den Grund zu gehen, bestimmten sie die Proteinstruktur des Rheb in seinem inaktiven Zustand.
Diese strukturellen Daten setzten die Wissenschaftler in Beziehung mit der Dynamik des Proteins, indem sie die Beweglichkeit des Rheb im Bereich der Pico- bis Nanosekundenzeitskala mittels Kernresonanzspektroskopie (NMR) untersuchten. „Dabei stellte sich wiederum überraschend heraus, dass im Gegensatz zum bisherigen Stand der Forschung die Flexibilität der für die Funktion des Rheb wichtigen so genannten Schalter I- und Schalter II-Regionen vom Aktivitätszustand dieses Proteins abhängt“, berichtet Stoll. Demnach verhält sich Rheb ebenso dynamisch wie das bereits gut charakterisierte Ras-Protein.
Keine Ähnlichkeit der Signalwege
Die Forscher stellten darüber hinaus eine Wechselwirkung von Rheb mit dem typischen Ras-Partner Raf-Kinase fest. „Diese Ergebnisse ließen uns zunächst eine Ähnlichkeit der Rheb- und Ras-Signalwege vermuten“, so Heumann. Sorgfältige NMR-Messungen zeigten jedoch klar, dass die Affinität zwischen Rheb und Raf-Kinase circa 1.000-mal niedriger ist als zwischen Ras und Raf-kinase.
„Eine physiologisch bedeutsame Wechselwirkung zwischen ihnen gibt es daher nicht“, folgern die Forscher. „Die Signalwege von Rheb und Ras sind offenbar weit voneinander entfernt.“ Durch die gezielte Unterdrückung der Bildung eines weiteren Signalproteins, der apoptosis signalling kinase-1 (ASK-1), konnten die Forscher beweisen, dass dieses maßgeblich und ursächlich an der von Rheb verstärkten Apoptose beteiligt ist.
Rapamycin mit Bedacht einsetzen
Diese Erkenntnisse sind nicht nur für die Grundlagenforschung bedeutsam. Mutationen in dem Rheb vorgeschalteten Signalkomplex verursachen so genannte tuberöse Sklerose, häufig auch als Bourneville-Pringle-Syndrom oder Bourneville-Brissaud-Pringle-Syndrom bezeichnet. Diese autosomal-dominante genetische Erkrankung geht den Forschern zufolge mit Fehlbildungen und Tumoren des Gehirns, Hautveränderungen und meist gutartigen Tumoren in anderen Organsystemen einher und führt häufig zu epileptischen Anfällen und kognitiven Behinderungen. Sie betrifft etwa eines von 8.000 Kindern.
In laufenden Studien, beispielsweise in den USA, erhofft man sich eine Verbesserung der Symptome durch Rapamycin. „Unsere Ergebnisse zeigen aber, dass Rapamycin auch gegenteilige Wirkung entfalten kann, wenn es auf gestresste Zellen einwirkt“, erklärt Heumann. „Der Zustand der Zelle ist entscheidend.“
(idw – Ruhr-Universität Bochum, 02.11.2010 – DLO)