Bei einer Infektion mit neuen, dem Körper unbekannten Grippeviren kann das menschliche Immunsystem rasch einen angeborenen Schutzmechanismus gegen die Erreger aktivieren. Dabei spielt ein Protein, kurz „Mx“ genannt, eine wichtige Rolle. Wie dieses Protein seine antivirale Wirkung entfaltet, haben Forscher jetzt geklärt und berichten darüber in „Nature“.
.
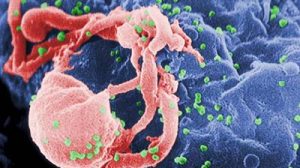
Neue Influenzaviren können ohne Vorwarnung immer wieder vom Tier auf den Menschen überspringen, wie die Erfahrungen mit dem H5N1-Vogelgrippevirus oder jüngst mit der Schweinegrippe belegen. Obwohl der Mensch meist keine Immunität gegen solche Erreger hat, ist sein Körper den Eindringlingen nicht schutzlos ausgeliefert. Er verfügt über eine rasch mobilisierbare Abwehr, die dafür sorgt, dass sich die Influenzaviren nicht ungehemmt vermehren können. Ein wesentliches Element dieses Schutzes besteht aus einem körpereigenen Protein, das eindringende Viren in der Zelle abfängt und daran hindert, Nachkommen-Viren zu produzieren.
Interferon löst Produktion des Schutzproteins aus
Unter normalen Umständen ist dieses Schutzprotein „Mx“ (Myxovirus-Resistenz) gar nicht in den Zellen vorhanden. Es wird erst kurzfristig nach Bedarf hergestellt, dann aber in großen Mengen. Der Befehl zur Herstellung wird durch den Botenstoff Interferon vermittelt, der von virusinfizierten Zellen ausgeschieden wird und dem Organismus den Virusbefall ankündigt.
Wie genau das schützende Protein die Virusvermehrung blockiert, war jedoch bisher nur ungenügend verstanden, weil dessen Struktur trotz jahrelanger Anstrengungen verschiedener Forschungsgruppen nicht aufgeklärt werden konnte. Virologen vom Freiburger Institut für Medizinische Mikrobiologie und Hygiene und Strukturbiologen vom Berliner Max-Delbrück-Centrum für Molekulare Medizin (MDC) ist es nun gelungen, neue strukturelle Einsichten zu gewinnen und daraus Voraussagen zur Wirkungsweise des antiviralen Proteins abzuleiten.
Struktur des „Stiels“ entschlüsselt
Das als „Mx“ bezeichnete Protein ist eine molekulare Maschine, die ihre volle Kraft erst nach Aneinanderlagerung der Einzelmoleküle zu einem hochmolekularen Verbund entfaltet, wobei sich Ringstrukturen ausbilden. Ein zentrales Element der Ringbildung besteht in der besonderen Faltung eines Teils von „Mx“, der als Stiel bezeichnet wird. Nach der genauen Struktur dieses Stiels wird seit Jahren gefahndet. Die beiden Forschergruppen entschlüsselten nun erstmals die Stiel-Struktur auf atomarer Ebene.
Die jetzt bekannte Struktur erklärt den Aufbau von „Mx“ und erlaubt testbare Voraussagen zur Funktionsweise des antiviralen Moleküls. Zusammen mit Ergebnissen aus früheren biochemischen Untersuchungen wird jetzt klar, dass „Mx“ mit der Stiel-Struktur eine Art Fußangel bildet, die wichtige Bestandteile des Influenzavirus in der infizierten Zelle fesselt und inaktiviert. Dass es dennoch bei dem Auftreten neuer Grippeviren zu Epidemien oder gar Pandemien kommen kann, hängt mit der Aggressivität und Massivität dieser Erreger zusammen.
Die Forscher sind zuversichtlich, mit ihren neuen Erkenntnissen über das schützende „Mx“-Protein die Grundlage für die Entwicklung neuer antiviraler Medikamente gegen die gefährlichen Influenzaviren gelegt zu haben. Sie sind zudem sicher, dass die an „Mx“ gewonnenen Erkenntnisse auch das Verständnis für weitere Mitglieder dieser Proteinfamilie erhöhen.
(Universität Freiburg, 29.04.2010 – NPO)