Eine Membranpore nie gekannten Ausmaßes haben jetzt Wissenschaftler in der Hülle eines Zellorganells, dem Peroxisom, entdeckt. Dieses „Scheunentor“ unter den Poren klärt auch die lange rätselhafte Frage, wie gefaltete mehrteilige Rieseproteine in die Peroxisomen gelangen. Dass dieses Tor der Superlative trotzdem jahrzehntelang unentdeckt bliebt, führen die Forscher in „Nature Cell Biology“ auf seine rasante Dynamik zurück.
Proteine müssen vom Entstehungsort bis hin zu ihrem Zielort oft Membranen durchqueren. Die Transportkanäle dafür sind meist sehr klein, nur ein bis zwei Nanometer im Durchmesser. Für den Import beispielsweise in die Mitochondrien müssen die Proteine daher entfaltet und dann schnurartig durch die Membran gefädelt werden. Erst auf der anderen Seite erhalten sie ihre fertige, räumliche Struktur. Die zugrunde liegenden Mechanismen vieler dieser Transportwege sind weitestgehend bekannt, doch es gibt eine Ausnahme, die Peroxisomen.
Rätsel der Riesenproteine
Diese Organellen kommen in fast allen Zellen vor und enthalten besonders große Proteine. Sie können nur deshalb um ein Vielfaches größer sein, da sie nicht entfaltet werden und oftmals aus mehreren Einheiten bestehen. Wie Peroxisomen jeodch diese riesigen Proteine importieren, war bislang ein Rätsel. „Besonders rätselhaft war, dass peroxisomale Proteine auf ihrem Weg eine Membran durchqueren, die als undurchlässig auch für die kleinsten chemischen Bausteine gilt“, erklärt Ralf Erdmann, Professor an der Medizinschen Fakultät der der Ruhr-Universität Bochum. Schon vor fünf Jahren hatten er und seine Kollegen postuliert, dass es in der Membran der Peroxisomen besonders große Poren geben muss, die die Proteine auch im gefalteten Zustand passieren lassen.
Suche nach dem „Scheunentor“
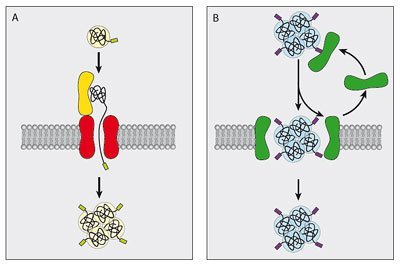
„Würde man die bekannten Transportkanäle als ‚Eingangstüren‘ in ihre Organellen bezeichnen, so würde man für die Peroxisomen eine Pore mit den Dimensionen eines ‚Scheunentores‘ erwarten“, erklärt Erdmann. Die Bochumer suchten nach diesem peroxisomalen Scheunentor, indem sie die Schlüsselkomponenten des Membrantransports auf eine künstliche Membran übertrugen. Neu hergestellte peroxisomale Proteine werden von Importrezeptoren in der Zellflüssigkeit erkannt und an die peroxisomale Membran dirigiert, wo die Proteine auf bislang unbekannte Weise über die Membran transportiert werden.
Der peroxisomale Importrezeptor Pex5p kommt in allen Zellen in zwei Zustandsformen vor: In löslicher Form in der Zellflüssigkeit und in einer integralen membran-gebundenen Form in Peroxisomen. Die Bochumer Gruppe untersuchte nun die Idee, dass der membrangebundene Rezeptor selbst integrativer Bestandteil eines kurzlebigen Kanals sein könnte, durch den dann das mitgeführte peroxisomale Protein die Membran passieren kann.
Tor in künstlicher Membran
Tatsächlich gelang es den Forschern nun, einen Membranproteinkomplex, der hauptsächlich aus Rezeptor und seinem Dockingprotein besteht, aus peroxisomalen Membranen der Bäckerhefe zu isolieren und in künstliche Membranen einzubauen. Unter Mitwirkung von Kollegen vom biophysikalischen Institut der Universität Osnabrück wiesen sie zunächst die Existenz eines dynamischen wassergefüllten Kanals nach. Dieser war allerdings nicht groß genug, um Proteine zu transportieren.
Es bedurfte eines Tricks, um die Pore weit zu öffnen: Dazu mussten die Forscher die Proteoliposomen mit gereinigten löslichen Rezeptorkomplexen aus der Zellflüssigkeit vorinkubieren. Dabei zeigte sich, dass der Kanal in Abhängigkeit von der Größe der Rezeptor-Cargo Komplexe sehr schnell seine Öffnungszustände ändern kann. Die größten Öffnungszustände wurden dabei mit über neun Nanometer Porendurchmesser gemessen.
Größte Proteinimport-Pore außerhalb des Kerns
„Wenn man von der Pore des Zellkerns absieht, handelt es sich um die größte jemals beobachtete Proteinimport-Pore“, verdeutlicht Erdmann. „Dass diese Pore über Jahrzehnte hinweg unentdeckt blieb, liegt wahrscheinlich an der ausgesprochenen Dynamik der ausgeklügelten Importmaschinerie von Peroxisomen, die dazu führt, dass der Eingang nur für kurze Zeit geöffnet und sofort wieder geschlossen wird.“
(Ruhr-Universität Bochum, 05.03.2010 – NPO)