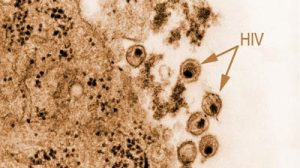
Eine neue Studie könnte möglicherweise erklären, warum nur eine von mehreren unabhängigen Übertragungen von Affen-Immundefizienzviren (SIV) aus Schimpansen auf den Menschen zur weltweiten AIDS-Pandemie führte. Das internationale Forscherteam konnte zeigen, dass es lediglich der HIV-1 Gruppe M (major), die weltweit für mehr als 90 Prozent aller Infektionen verantwortlich ist, gelungen ist, sich nach der Übertragung optimal an den neuen Wirt anzupassen.
{1r}
Nur HIV-1 M entwickelte ein voll funktionsfähiges so genanntes Vpu-Protein im Menschen, so die Wissenschaftler in der Fachzeitschrift „Cell Host & Microbe“. Vpu-Proteine der nichtpandemischen HIV-1 Gruppe O (outlier) und der sehr seltenen Gruppe N (non-M, non-O) dagegen sind entweder nicht in der Lage einen antiviralen Faktor namens Tetherin auszuschalten oder den Transport von CD4, dem primären Rezeptor der HI-Viren, zur Zelloberfläche zu verhindern. Die Forscher hoffen, dass diese Ergebnisse dazu beitragen, neue Wege zu finden, die Ausbreitung der AIDS-Viren zu verhindern.
Zum Schutz gegen retrovirale Infektionen produzieren menschliche Zellen so genannte Restriktionsfaktoren, die die effektive Virusvermehrung blockieren. Einer dieser antiviralen Faktoren wurde erst letztes Jahr von amerikanischen Forschern entdeckt und als Tetherin bezeichnet, weil er neu produzierte Viruspartikel an der Zelloberfläche „festhält“ und dadurch deren weitere Ausbreitung verhindert.
Eiweiß schaltet Tetherin aus
Allerdings hat HIV-1 M, der Haupterreger von AIDS, ein bestimmtes Eiweiß – das Vpu-Protein – entwickelt, das in der Lage ist Tetherin auszuschalten. Eine zweite Funktion des HIV-1 M Vpu-Proteins ist es, den primären Rezeptor der Immundefizienzviren, CD4, von der Zelloberfläche fernzuhalten umso zu verhindern, dass freigesetzte Viruspartikel direkt an die bereits infizierte Zelle zurückbinden. Vpu erhöht somit auf zweifache Weise die Effizienz der Virusfreisetzung.
Die Forscher um Professor Frank Kirchhoff von der Universität Ulm untersuchten in ihrer neuen Studie, ob auch die Vpu-Proteine von SIVcpz aus Schimpansen – dem direkten Vorläufer von HIV-1 – diese Funktionen ausüben können. Überraschenderweise fanden sie, dass SIVcpz nicht Vpu sondern ein anderes virales Eiweiß benutzt, das Nef-Protein, um Schimpansen-Tetherin auszuschalten. Die Tetherin-Variante, die man im Menschen findet, ist allerdings resistent gegen Nef, weil ihr in dem Bereich der sonst mit Nef interagiert fünf Aminosäuren fehlen.
Nur HIV-1 M konnte sich anpassen
„Direkt nach der Übertragung von SIVcpz auf den Menschen war das Virus somit nicht in der Lage Tetherin auszuschalten“, erläutert Kirchhoff. „Da menschliches Tetherin gegen Nef resistent ist, war HIV-1 gezwungen zu Vpu zu wechseln um diesen antiviralen Faktor zu eliminieren“. Lediglich dem Haupterreger von AIDS, HIV-1 M, gelang dies perfekt. Die Vpu- und Nef-Proteine der nicht pandemischen HIV-1 Gruppe O sind nicht in der Lage Tetherin zu antagonisieren.
Die Vpu-Proteine der sehr seltenen Gruppe N Viren haben zwar während der Anpassung an den Menschen anti-Tetherin-Aktivität erworben, jedoch dabei die Fähigkeit eingebüßt, den Transport des CD4 Rezeptors zur Zelloberfläche zu blockieren.
Die Ergebnisse zeigen nach Angaben der Wissenschaftler, dass es nur HIV-1 M gelungen ist, sich nach der Übertragung vom Schimpansen auf den Menschen optimal an den neuen Wirt anzupassen. Dies könnte ein wichtiger Grund dafür sein, warum nur eine von mehreren unabhängigen Übertragungen für den Großteil der AIDS-Pandemie verantwortlich ist.
(idw – Universität Ulm, 19.11.2009 – DLO)