Bei der Multiplen Sklerose schädigt das Immunsystem durch fehlgeleitete Aktivitäten nicht nur die Nervenhüllen, sondern auch die Nervenzellen selbst. Eine einzige T-Zelle kann dabei bis zu zehn Nervenzellen töten, wie Forscher aus Würzburg und Zürich erstmals experimentell nachgewiesen haben.
Entzündungen im zentralen Nervensystem können von Krankheitserregern wie Viren, aber auch vom Immunsystem des eigenen Körpers ausgelöst werden. Letzteres ist zum Beispiel bei der Multiplen Sklerose der Fall. Drastisch sind die Folgen einer solchen Entzündung: Es sterben die Zellen, die eine isolierende Hülle um die Nervenfasern herum aufbauen und intakt halten. Die Hüllen gehen ebenso verloren, und oft sterben schließlich auch die Nervenzellen selbst.
Tod der Nervenzellen entscheidend für Krankheit
„Bei Multipler Sklerose zum Beispiel nimmt man an, dass nicht nur der Verlust der Myelinhüllen, sondern vor allem der Tod der Nervenzellen entscheidend für die bleibenden Behinderungen ist, mit denen viele Patienten zu kämpfen haben“, erklärt Professor Heinz Wiendl von der Neurologischen Klinik der Universität Würzburg. Das seien Behinderungen wie Lähmungen oder eine eingeschränkte
Sehfähigkeit. Weltweit sind schätzungsweise 2,5 Millionen Menschen von der Multiplen Sklerose (MS) betroffen. In Deutschland leben nach aktuellen Hochrechnungen etwa 122.000 MS-Erkrankte. Heilbar ist die Multiple Sklerose bislang nicht; die Medizin kann aber die Symptome lindern und die Lebensqualität der Patienten verbessern.
Zwei Arbeitsgruppen haben nun zeitgleich erstmals beschrieben, dass bestimmte T-Zellen des Immunsystems nicht nur die myelinbildenden Zellen direkt beeinträchtigen, sondern auch „Kollateralschäden“ bei Nervenzellen oder deren Fortsätzen hervorrufen. Veröffentlicht wurden die Arbeiten in den Fachblättern „Glia“ und „American Journal of Pathology“.
Indirekter Effekt lässt Nervenzellen sterben
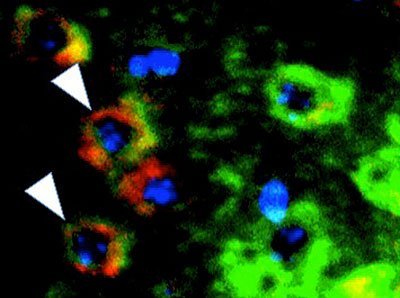
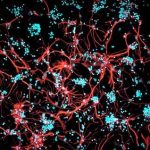
Wiendls Team von der Universität Würzburg gelang der Nachweis dieses Effekts anhand von Hirngewebekulturen: T-Zellen, die ausschließlich eine bestimmte Struktur auf der Oberfläche der myelinbildenden Zellen attackieren, verursachten darin innerhalb weniger Stunden auch einen signifikanten Untergang von Nervenzellen. Wie dieser indirekte Effekt zu Stande kommen könnte, erklärt der Würzburger Forscher Sven Meuth so: „Möglicherweise setzen die T-Zellen lösliche Faktoren frei, wie Perforin oder Granzym-B, die dann zu den Nervenzellen wandern und sie schädigen.“
Mord in Serie: Jede T-Zelle schlägt vielfach zu
Geradezu wie Serienkiller gehen die aggressiven T-Zellen dabei vor: „Eine einzige davon kann bis zu 30 myelinbildende Zellen und gleichzeitig bis zu zehn Nervenzellen töten“, so Wiendl. Diese T-Zellen schneiden die Fortsätze von Nervenzellen regelrecht durch. Das zeigte ein Forscherteam um Professor Norbert Goebels von der Universität Zürich in einem ähnlichen experimentellen Ansatz mit Videoanalysen.
Möglicher Angriffspunkt für neue Therapien
„Diese Ergebnisse helfen uns, die Entstehung von akuten und chronischen Schäden bei Entzündungen des zentralen Nervensystems besser zu verstehen“, erläutert Professor Wiendl. Auch die Patienten profitieren in der Zukunft möglicherweise von den Erkenntnissen – schließlich eignen sich die aggressiven T-Zellen als Angriffspunkt für neue Therapien. Darum wollen die Wissenschaftler noch möglichst viel Neues über die Serienkiller herausfinden.
(Universität Würzburg, 13.10.2009 – NPO)