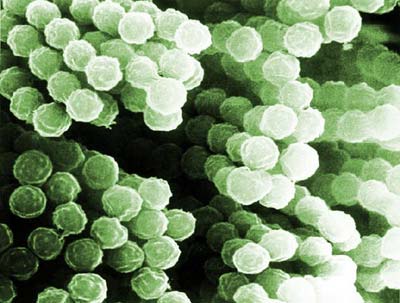
Ein internationales Wissenschaftlerteam hat herausgefunden, warum Pilzsporen beim gesunden Menschen keine Allergien oder Abwehrreaktionen hervorrufen. Die Sporen, von denen jeder Mensch täglich einige tausend einatmet, tragen auf ihrer Oberfläche ein Protein, das die Pilzzelle maskiert und vor der Antwort des menschlichen Immunsystems schützt.
Im Falle des krankheitserregenden Pilzes Aspergillus fumigatus handelt es sich um den Eiweißstoff RodA, der über Zuckermoleküle an die Zelloberfläche gebunden ist, berichten die Forscher aus Jena, Paris und Perugia im Wissenschaftsmagazin „Nature“.
Keine erkennbare Immunabwehr
Tagtäglich atmen wir einige tausend Pilzsporen ein. In der Nähe von Kompostieranlagen kann deren Zahl leicht eine Milliarde pro Kubikmeter überschreiten. Die Sporen dienen der Verbreitung der Schimmelpilze durch die Luft und werden bei bestimmten Pilzgruppen auch als Konidien bezeichnet. Sie enthalten viele Substanzen, vor allem Proteine und Zuckerverbindungen, die für den menschlichen Organismus fremd sind und daher vom Immunsystem erkannt und bekämpft werden sollten. Dem ist jedoch nicht so. Es kommt in der Regel weder zu einer erkennbaren Immunabwehr, noch zu allergischen Reaktionen.
Pilze als Opportunisten
Andererseits erkranken gesunde Menschen normalerweise nicht an Pilzinfektionen der Lunge, die Sporen können also dort nicht auskeimen und sich ansiedeln. Nur wenigen krankheitserregenden Pilzen gelingt dies. Es handelt sich hierbei jedoch um so genannte Opportunisten, die nur dann infektiös sind, wenn der Mensch bereits an anderen Erkrankungen leidet und seine Immunabwehr geschwächt ist.
Forscherteams um Axel Brakhage vom Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie – Hans-Knöll-Institut – und der Universität Jena und seine Kollegen Jean-Paul Latgé vom Pariser Institut Pasteur und Luigina Romani von der Universität Perugia haben nun herausgefunden, woran das liegt. Sie untersuchten verschiedene über die Luft verbreitete Pilze, darunter auch den für den Menschen gefährlichen Schimmelpilz Aspergillus fumigatus.
Charakteristisches Protein identifiziert
Dabei haben die Wissenschaftler ein charakteristisches Protein aus der Oberfläche der Pilzsporen identifiziert. Das als RodA bezeichnete hydrophobe, also wasserabweisende Eiweiß ist immunologisch völlig inaktiv. Versuche mit isolierten Immunzellen und mit Mäusen zeigten, dass RodA weder Alveolarmakrophagen noch dendritische Zellen oder T-Helferzellen aktiviert.
Alveolarmakrophagen sind eigentlich dafür verantwortlich, Fremdkörper wie Bakterien, Viren oder eben Pilzsporen in der Lunge zu erkennen, in sich aufzunehmen und damit unschädlich zu machen. Dendritische Zellen und T-Helferzellen sind an der Regulation des Immunsystems bei Säugetieren beteiligt und sorgen unter anderem für Entzündungsreaktionen und die Bildung spezifischer Antikörper, die Eindringlinge erkennen und markieren.
Eiweiß umhüllt Pilzsporen
Aus diesen Ergebnissen leiteten die Wissenschaftler die Hypothese ab, dass das Eiweiß RodA die Pilzsporen wie eine Hülle umgibt und die Sporen gewissermaßen maskiert, so dass die Immunreaktion des Menschen unterbleibt.
Zur Bestätigung dieser Vermutung entfernten die Forscher durch chemische Behandlung das Protein von den Sporen. Außerdem erzeugten sie Mutanten des Pilzes, denen die Fähigkeit zur Bildung von RodA fehlte. In anschließenden Tierversuchen zeigte sich, dass die in der Oberflächenstruktur veränderten Pilzzellen plötzlich hochgradig immunologisch aktiv waren. So wanderten Immunzellen massenhaft in das behandelte Lungengewebe ein. Außerdem wurde die Ausschüttung von Botenstoffen – so genannten Chemokinen – registriert, die an Entzündungsreaktionen beteiligt sind. Auch die bereits erwähnten Alveolarmakrophagen wurden aktiviert und begannen, die ihrer Maskierung beraubten Konidien aufzunehmen und zu verdauen.
Kommunikation zwischen Mensch und Mikrobe
Die Ergebnisse zeigen nach Angaben der Forscher, dass die gemeinsame Evolution von Mikroorganismen und Säugern in diesem Fall für beide Seiten Vorteile bringt: Die Sporen bleiben zunächst unerkannt und erhalten somit Gelegenheit, in der Lunge des Wirtes auszukeimen und sich einen für sie günstigen Lebensraum zu erschließen – mit möglicherweise fatalen Folgen für den betroffenen Patienten. Andererseits reagiert das menschliche Immunsystem nicht bei jedem Kontakt mit Mikroorganismen mit einer starken Aktivierung, die sich in allergischen Reaktionen oder einer Entzündung äußern würde.
Erst dann, wenn die Konidien des Pilzes beginnen auszukeimen und das menschliche Gewebe zu besiedeln, ist eine effektive Erkennung und Abwehr durch das Immunsystem erforderlich. Da die Sporen während der Keimung das Protein RodA verlieren, steht diesem Prozess nichts im Wege. Das Beispiel zeigt, so die Forscher, wie fein ausbalanciert die Kommunikationsprozesse zwischen Mensch und Mikrobe sind und wie schmal der Grat sein kann, der zwischen der natürlichen Widerstandskraft gegen eine Krankheit und dem Ausbruch einer Infektion verläuft.
(idw – Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie – Hans-Knöll-Institut (HKI), 24.09.2009 – DLO)